Наночастицы и нанокомпозитные структуры на их основе в последнее время все больше попадают под пристальное внимание ученых и инженеров. Успехи, которых достигла в настоящее время технология изготовления наночастиц, позволяют изготавливать наночастицы радиусом в несколько нанометров сферической и эллипсоидальной формы, а также наночастицы сложной структуры с оболочкой. Наночастицы и нанокомпозитные материалы на их основе находят применение для изготовления твердотельных устройств фотоники и оптоэлектроники, таких как фильтры, усилители, а также могут использоваться в качестве высокоэффективных высокочувствительных сенсоров [7]. Наночастицы из металла или наночастицы с металлической оболочкой, обладающие поверхностным плазмонным резонансом, находят применение в разных областях науки и техники, таких как химия, физика, биология, медицина, нанотехнологии, биотехнологии и т.д. Большим потенциалом для использования в биологии и медицине обладают также магнитные наночастицы. Благодаря высокой удельной намагниченности и возможности связывания на поверхности биологических молекул магнитные наночастицы на основе оксида железа являются перспективным материалом для разработки селективных контрастирующих агентов для магнито-резонансной томографии [6]. Для решения биохимических задач различной степени сложности необходимо сочетание магнитных свойств и особых свойств поверхности, которые наблюдаются у наночастиц. Наночастицы магнетита, функционализированные биомолекулами (антителами, ферментами, нуклеотидами и др.) для нацеливания или узнавания биологических систем, могут быть использованы в качестве материалов для адресной доставки лекарственных препаратов [6].
Особого внимания заслуживают наночастицы типа ядро–оболочка, обладающие способностью комбинировать свойства нескольких материалов в одной частице. Так, использование магнетита в качестве ядра для материалов типа ядро–оболочка позволяет избежать всех недостатков, которые демонстрируют коллоидные растворы наночастиц оксида железа. Они являются токсичными, демонстрируют склонность к быстрой агрегации в различных биологических растворах, трудность функционализации поверхности [6]. Для преодоления этих недостатков можно использовать наночастицы с оболочкой. В качестве оболочки используют неорганические материалы, обеспечивающие стабильность, простоту функционализации поверхности и биосовместимость. Подходящим и оптимальным материалом для образования оболочки наночастиц является золото, обладающее биосовместимостью и высокой стабильностью [6].
Коллоидные растворы частиц золота малых размеров использовали в лечебных целях еще в древнейшие времена. Однако, лишь в последние десятилетия, благодаря появлению новых данных об уникальных оптических и физико-химических свойствах золотых наночастиц, началось их активное применение в различных биологических, медицинских целях как в экспериментальной биологии и медицине, так и на практике [4].
Интерес к золотым и другим частицам благородных металлов (например, наночастицам из серебра) обусловлен их уникальными оптическими свойствами, связанными с возбуждением локализованных плазмонных резонансов в металлических наночастицах, взаимодействующих со светом [4]. Эти возбуждения поверхностных плазмонов приводят к целому классу плазмонно-усиленных линейных свойств, таких как резонансное поглощение, рассеяние, генерация сильных локальных полей, гигантское комбинационное рассеяние [4].
В нанотехнологии, которая находит применение в биомедицинских исследованиях, применяются золотые и серебряные наночастицы, которые хорошо адсорбируют различные биологические реагенты. Так, к металлическим наночастицам можно прикрепить биологические макромолекулы, молекулы, работающие в качестве зонда, например, антитела. Наноструктуры, содержащие наночастицу в качестве ядра с прикрепленными к ним биологическими молекулами, называют биоконъюгатами или конъюгатами. При этом прикрепление биомакромолекул к наночастицам называется функционализацией [4]. В таком случае биомакромолекула конъюгата используется для того, чтобы прикрепиться к биологическому объекту, который является мишенью. Золотые наночастицы находят широкое применение в биомедицине также из-за хорошей биологической совместимости, низкой химической реакционной способности, а также из-за хорошей функционализации. Однако некоторые металлы, например, серебро, могут демонстрировать высокую химическую активность, поэтому такие металлические наночастицы, которые работают на основе поверхностного плазмонного резонанса, необходимо окружать оболочкой из диэлектрика, которая будет защищать их от контакта с биологической анализируемой средой. Таким образом, для практических применений подходят наночастицы с оболочкой: диэлектрические наночастицы с оболочкой из золота, обеспечивающие хорошую функционализацию, или металлические наночастицы с диэлектрической оболочкой, предотвращающей химический контакт с аналитом. Однако необходимо помнить о том, что увеличение толщины диэлектрической оболочки наночастиц приводит к уменьшению чувствительности, то есть к уменьшению сдвига максимума плазмонного резонанса при изменении показателя преломления анализируемого раствора. Поэтому важной задачей является оптимизация параметров наночастиц и подбор их геометрических размеров и толщины оболочки, которые обеспечат повышение чувствительности спектрального сдвига максимума поверхностного плазмонного резонанса.
Для задач биомедицины применяются полупроводниковые наночастицы, которые могут использоваться в качестве люминесцентных зондов или меток, находящих применение, например, для флуоресцентной томографии. Причем использование полупроводниковых наночастиц с оболочкой из более широкозонного полупроводника приводит к усилению люминесценции.
В данной работе рассматриваются наночастицы сферической формы, имеющие полупроводниковое ядро, окруженные металлической оболочкой. Диэлектрическая проницаемость металла рассматривается в рамках модели Друде и выражается следующей формулой:
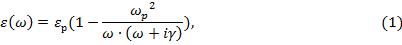
где eр – решеточная часть диэлектрической проницаемости,
wр – плазменная частота для металла,
g - столкновительная частота для металла. Столкновительная частота определяет наличие затухания в среде.
Тензор диэлектрической проницаемости полупроводника записывается в известном виде [1]:
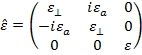 , (2)
, (2)
где компоненты тензора диэлектрической проницаемости имеют следующий вид [3]:
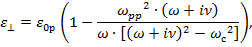
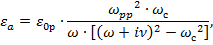
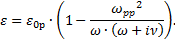
Здесь wрр – плазменная частота для полупроводника,
wс – циклотронная частота,
n - столкновительная частота для полупроводника,
e0р – решеточная часть диэлектрической проницаемости для полупроводника.
Результаты расчета частотной зависимости компонент тензора диэлектрической проницаемости модельного полупроводника представлен на рисунках 1 и 2.
Из рисунков 1 и 2 видно, что зависимость компонент тензора диэлектрической проницаемости e^ и eа от частоты носит сложный характер. При определенной частоте, зависящей от циклотронной частоты wс, наблюдается смена знака у компонент тензора. Если ядро наночастицы выполнено из полупроводника, то такое изменение знака компонент e^ и eа приводит к изменению частоты поверхностного плазмонного резонанса на границе раздела с металлической оболочкой и даже к возникновению новых частот поверхностного плазмонного резонанса.
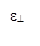
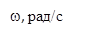
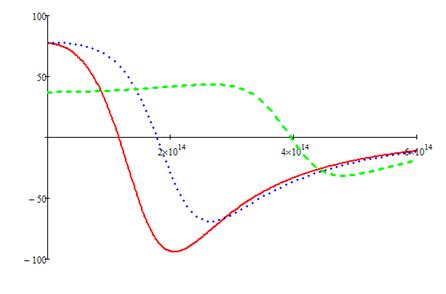
Рис.1. График зависимости компоненты тензора e^ диэлектрической проницаемости полупроводника от частоты. Сплошная кривая: wс=1,5×1014 рад/с, точечный пунктир: wс=2×1014 рад/с, длинный пунктир: wс=4×1014 рад/с
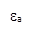
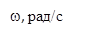
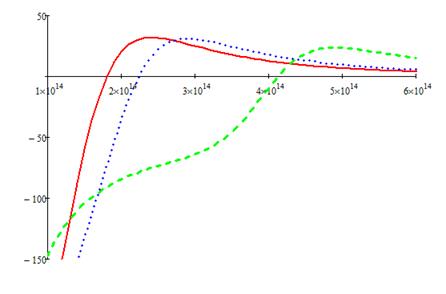
Рис.2. График зависимости компоненты тензора eа диэлектрической проницаемости полупроводника от частоты. Сплошная кривая: wс=1,5×1014 рад/с, точечный пунктир: wс=2×1014 рад/с, длинный пунктир: wс=4×1014 рад/с
Циклотронная частота для полупроводника вычисляется следующим образом (в системе СГС):

где Н – напряженность внешнего магнитного поля.
Так как циклотронная частота полупроводника зависит от величины внешнего магнитного поля, то, меняя магнитное поле, можно изменять частоту поверхностного плазмонного резонанса в наночастицах с металлической оболочкой. Таким образом, наночастицы с оболочкой и полупроводниковым ядром обладают следующим важным свойством: электродинамическими параметрами таких наночастиц можно управлять, меняя величину внешнего магнитного поля.
Нахождение положения максимума поверхностного плазмонного резонанса, который наблюдается на сферической границе раздела полупроводник – металл, является сложной задачей, которая не имеет аналитического решения. Для численного определения частоты поверхностного плазмонного резонанса проведем расчет сечения поглощения наночастицы с металлической оболочкой в соответствии с методикой, описанной в работах [2], [5]. Результаты расчета сечения поглощения представлены на рисунке 3.
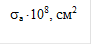
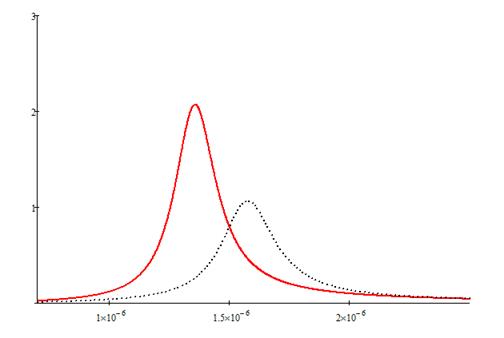
Рис.3. Расчет сечения поглощения полупроводниковой наночастицы с золотой оболочкой. Радиус ядра 27 нм, толщина оболочки 17 нм. Сплошная кривая: wс=1,5×1014 рад/с, точечный пунктир: wс=2×1014 рад/с
Из рисунка 3 хорошо видно, что увеличение циклотронной частоты полупроводника от 1,5×1014 рад/с до 2×1014 рад/с, наблюдаемое при увеличении внешнего магнитного поля, приводит к сдвигу максимума поверхностного плазмонного резонанса от 1,35 мкм до 1,58 мкм.
Выводы
В работе исследуются наночастицы с оболочкой, которые могут применяться в качестве сенсоров для биологических и медицинских исследований. Рассмотрены наночастицы, состоящие из полупроводникового ядра и металлической оболочки. С учетом диэлектрической проницаемости металла, рассчитываемой в рамках модели Друде, и частотной зависимости компонент тензора диэлектрической проницаемости полупроводника проведены расчеты сечения поглощения рассматриваемых наночастиц с золотой оболочкой. Показано, что изменение магнитного поля влияет на положение поверхностного плазмонного резонанса в наночастицах. Полученные в работе результаты могут использоваться для создания контрастирующих агентов для магнито-резонансной томографии или в качестве биологических меток.

