Глава 1
Этиология, патофизиология, факторы риска
Молекулярная биология и цитогенетика
В норме антигенная стимуляция зрелых В-клеток приводит к их пролиферации и дифференцировке в В-клетки памяти и плазмобласты. Плазмобласты в конечном счёте дифференцируются в короткоживущие плазматические клетки, которые остаются в локальных областях и умирают в течение трёх дней. Иммуноглобулин, синтезируемый короткоживущими плазмоцитами, не связан с соматическими гипермутациями и структурно является мономером IgM и имеет специальное название — BCR (B-Cell Receptor), в ряде случаев может происходить переключение типа синтезируемого иммуноглобулина (IgG, IgA и др.) с помощью специального вида рекомбинации — CSR (class switch recombination). Активированные В-клетки входят в герминативные центры лимфатических узлов и селезёнки, где происходят процессы V(D)J-рекомбинации, антигенная селекция и апоптоз. В результате плазмобласты, подвергшиеся переключению изотипа иммуноглобулинов, обычно мигрируют в костный мозг, где они взаимодействуют со стромальными клетками и под воздействием различных цитокинов дифференцируются в долго живущие плазмоциты. Продолжительность их жизни составляет в среднем 30 суток. Таким образом существуют следующие особые механизмы рекомбинации, использующиеся при созревании B-лимфоцитов: соматическая гипермутация (somatic hypermutation — HSM), переключение типа (class switch recombination — CSR) и V(D)J.
Антитела представляют собой гликопротеиды, которые состоят из четырёх цепей: двух одинаковых тяжелых цепей (H-chains) и двух легких (L-chains). Вместе они образуют структуру, похожую на латинскую букву Y. Каждая “ветка” этой буквы — это одна легкая цепь, соединённая дисульфидными связями с амино-терминальной частью тяжелой цепи. А “ствол” — это две спаренные карбоксильные части двух тяжёлых цепей, которые так же соединены между собой дисульфидными связями. Полипептидные цепи могут сильно отличаться по аминокислотному составу, и все эти отличия находятся в одном участке — (гипер)вариабельный участок или V-region; VH обозначает такой участок для тяжёлой цепи, VL - для лёгкой. Два таких участка, один из тяжелой цепи, другой из лёгкой, образуют антиген-связывающий сайт. У каждого Y-образного антитела есть два таких антиген-связывающих участка, расположенных на концах каждой “ветки”. Остальные части легких и тяжелых цепей не так разнообразны в аминокислотном составе, поэтому называются константные (каркасные) участки или C-regions. Участки, которые расположены на “ветках”, называются Fab (Fragment antigen binding), потому что они связываются с антигеном. Участок, который расположен на “стволе”, называется Fc (Fragment crystallizable), потому что он легко кристаллизуется, отвечает за функции молекулы антитела, реагируя с сывороточными белками и рецепторами клеточной поверхности. Разница в С-регионах тяжёлых цепей даёт нам пять главных изотипов (или классов) иммуноглобулинов, которые играют свои роли в иммунном ответе. Это иммуноглобулины G, M, A, D и Е (IgG, IgM, IgA, IgD и IgE соответственно). Их тяжёлые цепи названы соответствующими строчными греческими буквами: (гамма (γ), мю (μ), дельта (δ), альфа (α), и эпсилон (ε), соответственно). У лёгких цепей всего два изотипа: каппа (κ) и лямбда (λ). Однако каждое антитело может иметь либо κ, либо λ тип лёгких цепей, не оба сразу. Относительное содержание разных типов лёгких цепей зависит от вида животных: например, у людей две трети всех антител содержат каппа цепи и всего одна треть лямбда цепи.
У людей, гены иммуноглобулина распределены следующим образом: локус тяжёлой цепи на 14-ой хромосоме, локус κ L-цепи на 2-ой хромосоме, а локус λ L-цепи на 22 хромосоме. Разные сегменты генов (есть для всех цепей) кодируют соответствующие участки: С-область (C), V-область (V) и лидирующий пептид (leader peptide — L). [7]
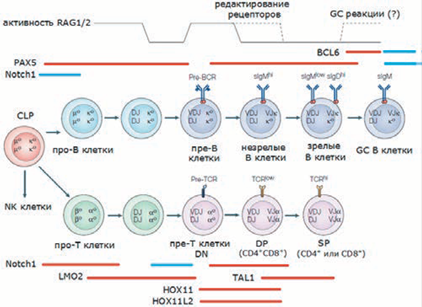
Для обеспечения необходимой точности при рекомбинации, все вариабельные сегменты снабжены специальными метками — RSS. Собранные рецепторы экспрессируются на мембранах и, если они функциональны, то внутриклеточные эффекторы сигнализации подавляют дальнейшую рекомбинационную активность в клетке, предотвращая рекомбинации на гомологичных парах хромосом (так называемое аллельное исключение). В редких случаях в незрелых В-клетках может снова стимулироваться RAG1\2-активность, которая приводит к новому ряду рекомбинаций в Ig-κ и\или Ig-λ-локусах хромосом, что приводит к редактированию рецептора. На рисунке можно увидеть активность V(D)
J-рекомбинации и стадии развития лимфоидных клеток. Показаны основные стадии развития В- и Т-клеток с указанием рекомбинационных процессов (DJ, VDJ, VJ) и экспрессирующихся на поверхности клеток BCR- (sIg) и TCR-рецепторов. Сверху представлен уровень активности RAG1/2 комплекса.
Сочетание сложности кариотипа и теломерная локализация некоторых транслокаций замедляют идентификацию трансформации при моноклональной гаммапатии и множественной миеломе. При изучении роли геномной нестабильности показано, что гиподиплоидность ассоциируется с более плохим прогнозом, чем гипердиплоидность [1]. Различают первичные хромосомные транслокации, связанные с начальным событием в онкогенезе, и вторичные (c-myc и др.), возникающие в поздний период развития заболевания и ассоциированные с опухолевой прогрессией. Также, в нескольких исследованиях показано, что в большинстве случаев множественной миеломы происходит транслокация генов тяжелых цепей. Транслокация Igλ происходит в 10% случаев МГ и в 20% при ММ, а Igκ происходят еще реже. Онкогенез в опухолях лимфоидного происхождения обычно происходит следующим образом: протоонкогены, попадающие в локусы BCR в результате хромосомных транслокаций избегают строгого клеточного контроля (т.е. превращаются в онкогены) и генерируют развитие опухолеродного процесса. Различают 5 онкогенов, которые вовлечены в транслокацию генов IgH при МГ и ММ: 11q13 (циклин D1), 6p21 (циклин D3), 4p16 (рецептор фактора роста фибробластов и предположительно гистоновая метилтрансфераза, участвующая в ремоделировании хроматина), 16q23 (c-maf) и 20q11 (mafB). Большинство транслокаций с 5 вышеуказанными онкогенами являются первичными и связаны с ошибками в рекомбинации в switch-регионе генов тяжёлых цепей. При изучении профиля генной экспрессии выяснилось, что мРНК циклинов D1, D2, D3 у больных ММ и МГ определённо выше, чем в нормальных плазматических клетках, но сравнимы с уровнями экспрессии циклина D2 в нормальных пролиферирующих плазматических клетках. Нормальные гемопоэтические клетки (В-лимфоциты, плазматические клетки и плазмобласты) экспрессируют циклины D2 и\или D3, но почти совсем не экспрессируют D1. Таким образом, наличие транслокаций генов, которые дисрегулируют работу циклина D1 или D3 (что происходит у 20% больных ММ), экспрессия циклина D1 в 40% случаев ММ и увеличенные во всех остальных случаях уровни циклина D2 свидетельствуют о дисрегуляции как минимум одного из генов циклинов, что может играть роль объединяющего онкогенного события при парапротеинемиях. (Примечание: циклины — это консервативная группа белков, ответственных за переход клетки из одной фазы цикла в другую. При помощи белков группы циклина D, клетка переходит из фазы G1 в S и G2). На основе результатов цитогенетических исследований, в 2004 году была предложена модель молекулярного патогенеза, в которой рассматриваются два пути превращения клетки. Первый путь связан с негипердиплоидными опухолями с очень высокой частотой транслокации IgH, вовлекающих 5 онкогенов и относительно высокой частотой потери части хромосомы 13/13q14. Второй механизм патогенеза характерен для гипердиплоидных опухолей и связан с множественными трисомиями, вовлекающими хромосомы 3, 5, 7, 9, 11, 15, 19 и 21, но реже встречающейся потерей части хромосомы 13/13q14 и транслокаций IgH с 5 онкогенами. Почти у половины опухолевых клеток первичная хромосомная транслокация приводит к дисрегуляции экспрессии циклинов, что может наделять клетки большей восприимчивостью к пролиферативным стимулам, приводящим к селективной экспансии. Это может происходить из-за неправильного и чрезмерного стимулирования мутантных клеток с цитокинами (IL-6). Адгезивные молекулы (такие как CD44, VLA-4, VLA-5, LFA-1, CD11a, CD56, CD138, MPC-1) способствуют хоумингу опухолевых клеток в костном мозге. Интересен тот факт, что у этих молекул также есть важные клинические и функциональные последствия. CD138 (Синдекан-1) регулирует рост и выживаемость опухолевых клеток, отсюда неудивителен тот факт, что его увеличение его концентрации в сыворотке крови свидетельствует о большой массе злокачественных клеток и коррелирует с плохим прогнозом. Связывание клеток через VLA с EMC-протеином способствует запуску генетических изменений, которые приводят к лекарственной резистентности.
Таким образом, одной из предпосылок развития опухолевых клеток является возникновение ошибок в естественном процессе развития плазмоцитов. Транслокации в гене тяжелой цепи и генах циклинов являются одними из ранних онкогенных событий, на поздних же этапах происходят вторичные изменения, такие как c-myc, p53 и другие. Они закрепляют злокачественные изменения клона и способствуют прогрессированию заболевания. Уточнение механизмов, благодаря которым злокачественная клетка выживает и размножается, может помочь в разработке новых перспективных подходов к лечению и ведению больных с гемобластозами.
Глава 2
Диагностика множественной миеломы
На сегодняшний день методы диагностики множественной миеломы включают в себя следующие: анамнез и жалобы больного, клинический анализ крови, биохимический анализ крови (с подсчётом уровней креатинина сыворотки, кальция, β2-микроглобулина, С-реактивного протеина, ЛДГ и альбумина сыворотки), общий анализ мочи, электрофорез белков плазмы крови и мочи, иммунофиксация тяжёлых и лёгких цепей, аспирация и биопсия костного мозга, лучевая диагностика (рентген исследование, магнитно-резонансная томография, компьютерная томография, позитронно-эмиссионная томография). Результаты цитогенетического исследования играют большую роль для составления прогноза и выбора тактики лечения. Основными методами здесь являются стандартное кариотипирование и FISH-анализ. Наиболее значимые аномалии это del(13q), t(4; 14) и del(17p), которые связывают с плохим прогнозом. Национальные клинические рекомендации по диагностике и лечению множественной миеломы дают следующие критерии установления диагноза:
1. Плазматические клетки в костном мозге 10% и более и/или плазмоклеточная опухоль в биопсийном материале пораженной ткани.
2. Моноклональный белок в сыворотке крови и/или в моче (за исключением пациентов с несекретирующей ММ).
3. Один или более следующих признаков поражения органов или тканей, связанных с плазмоклеточной пролиферацией:
— гиперкальциемия (> 11,5 мг/дл [> 2,65 ммоль/л]),
— почечная недостаточность (креатинин > 2 мг/дл [> 177 мкмоль/л]),
— анемия (Hb < 10 г/дл или на 2 г/дл ниже нормального уровня Hb),
— поражение костей (остеолитические поражения, остеопороз или патологические переломы) [3, [4], [6].
Лучевые методы диагностики
К лучевым методам диагностики относят рентген-диагностику, магнитно-резонансную томографию, компьютерную томографию, позитронно-эмиссионную томографию и их сочетания. Основным клиническим симптомом ММ являются разнообразные поражения костей. Механизмы костной деструкции заключаются в усилении резорбции костей под действием остеокластов, что сопровождается истощением функции остеобластов и угнетением костеобразования. При этом, прогрессирование поражения скелета наблюдается даже у пациентов, положительно отвечающих на химиотерапию. Таким образом, характерной чертой миеломного поражения костей является тот факт, что очаги поражения редко исчезают даже у пациентов, находящихся в полной ремиссии.
В трубчатых костях имеется ряд признаков, такие как “шелушение” эндоста, наличия отдельных мелких очагов лизиса, сливных участков из мелких и крупных деструктивных очагов. На рентгенограммах, как правило, можно увидеть диффузный остеопороз, который лучше всего виден в позвоночнике. Рекомендуемыми исследованиями в рутинной практике являются радиографическое исследование черепа, позвоночника, плечевых костей, рёбер, таза и бедренных костей. По классификации патологии плазматических клеток, пациенты с поражением костей относятся в категорию “манифестных” и требуют лечения даже при отсутствии клинических симптомов. К достоинствам РИ следует отнести:
1) Дешевизна и простота проведения
2) Использование низкодозной РИ всего тела так же эффективно, как КТ или МРТ в плане диагностики очаговых поражений.
К недостаткам относятся:
1) Ограниченная чувствительность метода и невозможность ранней диагностики.
2) Недостаточная специфичность — невозможно достоверно дифференцировать остеопороз, вызванный миеломой от остепороза другого генеза.
3) Интерпретация рентгенограмм может варьировать в зависимости от техники выполнения и квалификации врача.
4) Необходимость выполнения большого количества снимков, что увеличивает получаемую пациентом дозу излучения.
5) Неудобство для пациента, связанное с сильными болями. При проведении многочисленных снимков необходимо часто поворачивать или ставить пациента в разнообразные положения, что провоцирует болевые ощущения.
6) Невозможность оценить эффективность терапии. Это связано с тем, что очаги лизиса не исчезают в ответ на терапию.
Метод компьютерной томографии основан на послойном облучении организма рентгеновскими лучами, последующей регистрацией и обработкой ответа на компьютере. Он позволяет выявить мелкие очаги остелизиса при ММ, которые не видны на обычных рентгенограммах, является гораздо более чувствительным методом и позволяет получать трёхмерные изображения.
К преимуществам КТ перед РИ относят:
1) Длительность процедуры существенно меньше.
2) Нет необходимости перекладывать пациентов и делать большое количество снимков.
3) Диагностическая ценность существенно выше. КТ позволяет обнаружить большее количество очагов.
4) Более точная оценка риска переломов.
5) Возможность выявить параллельные патологические процессы.
Следует заметить, что компьютерная томография позволяет получить сведения только об анатомическом строении, но не о функциях. Из недостатков КТ следует отметить высокую дозу облучения, которая может быть в 1.3-3 раза выше, чем при стандартной рентгенографии.
Использование передовых методов сканирования скелета определённо способно улучшить раннюю диагностику асимптоматического течения миеломы. И магнитно-резонансная томография, в сравнении с РИ, является более чувствительным методом. МРТ позволяет визуализировать костномозговую полость и напрямую оценить степень миеломатозной инфильтрации еще до того, как на обычных рентгенограммах станет видна костная деструкция, причем без воздействия облучения. Также МРТ является методом выбора при подозрении на компрессию спинного мозга и при прогнозировании риска переломов позвоночника. В целом, преимущества МРТ перед РИ и КТ включают:
— Более высокая чувствительность метода;
— Возможность различия между ММ и здоровым костным мозгом;
— Возможность диагностики компрессии спинного мозга и нервных корешков;
— Подходит для оценки статуса моноклональной гаммапатии, бессимптомного течения ММ и при солитарных плазмоцитомах.
При поражении костного мозга миеломой выделяют пять типов МРТ картин:
1) Нормальный внешний вид костного мозга, несмотря на микроскопически обнаруживаемую плазмоклеточную инфильтрацию (~30%);
2) Фокальное поражение (~30%);
3) Гомогенная диффузная инфильтрация; (~25%)
4) Комбинированная диффузная и фокальная инфильтрация (~10%);
5) Картина с негомогенным костным мозгом и вкраплениями жировой ткани. (3-5%)
Также описана корреляция между диффузной и фокальной МРТ-картиной и низкими уровнями гемоглобина в сыворотке и высоким процентом плазмоцитов в костном мозге. Как правило, это свидетельствует о высокой опухолевой нагрузке. Однако основной методологической проблемой МРТ является недостаток специфичности выявляемых аномалий. Все найденные изменения не являются патогномоничными и могут как присутствовать, так и отсутствовать на момент диагностики. Также они могут быть вариантом нормы или представлять другой патологический или патофизиологический процесс, например, гемосидероз или реактивную гиперплазию костного мозга.
В последние годы для визуализации множественной миеломы также используется позитронно-эмиссионная томография. Этот метод основан на поглощении клетками радиофармпрепаратов (РФП) и последующей регистрации пары гамма-квантов, которые возникают при позитронном бета-распаде радионуклида. Выбор подходящего РФП позволяет изучать метаболизм, транспорт веществ и другие процессы, вплоть до экспрессии генов. При диагностике ММ РФП выбора является 18-фтор-деоксиглюкоза, которая поглощается метаболически активными клетками, что затем становится видно на сканограммах. Основным ограничением ПЭТ является небольшое разрешение. Так, очаг лизиса менее 1 сантиметра, который виден на обычных рентгенограммах, может не визуализироваться на ПЭТ. Поэтому чаще применяется сочетание ПЭТ\КТ, что решает проблему ограниченного разрешения и сочетает преимущества обоих методов. Чувствительность ФДГ-ПЭТ в плане выявления миеломатозного поражения является 85%, а специфичность — 92%. Подобная характеристика позволяет применять ПЭТ\КТ для диагностики и мониторинга несекретирующих миелом и миелом высокого риска. Помимо демонстрации персистирующего или рецидивирующего поражения костей, диагностика методом ПЭТ/КТ более чувствительна для локализации экстрамедуллярных очагов болезни, где она выявляет дополнительные очаги почти у 30% больных, у которых на МРТ был поставлен диагноз солитарной плазмацитомы. Однако наибольшую результативность показывает сочетание МРТ и ПЭТ\КТ, так как последнее может не выявить поражение костного мозга, а МРТ не показывает функциональную активность тканей.
Анализ мочи
Все виды парапротеинемических гемобластозов, и множественная миелома в том числе, характеризуются выделением аномальных белков с мочой. Качественные пробы на белок в моче основаны на способности белков подвергаться денатурации под влиянием разных физических и химических факторов. При наличии белка в исследуемом образце мочи появляется либо помутнение, либо выпадение осадка или хлопьев. Однако, как показывают многочисленные исследования, ни один из известных методов определения белка в моче не позволяет получать надежные воспроизводимые результаты.
2. Количественные методы. Точное определение количества белка в моче сопряжено с определенными трудностями:
• Низкое содержание белка в моче здорового человека;
• Присутствие различных соединений, способных повлиять на результат исследования;
• Различные вариации содержания и состава белков при различных заболеваниях, что ведёт к определенным сложностям с выбором калибровочного материала.
Идеальный метод количественного определения белка в моче должен удовлетворять следующим требованиям:
• Результат не должен зависеть от белкового состава исследуемого образца;
• Метод должен быть прост, не требовать высокой квалификации исполнителя, небольшое количество этапов;
• Обладать высокой чувствительностью;
• Быть устойчивым к воздействию различных факторов, таких как: присутствие лекарственных препаратов, колебания состава образца и др.
• Обладать приемлемой стоимостью;
• Быть легкоадаптируемым к автоанализаторам [2].
Широкое распространение получили методы определения белка в моче, основанные на способности различных красителей образовывать комплексы с белками. Наиболее популярными в настоящее время являются краситель Понсо, Кумасси бриллиантовый синий (КБС) и пирогаллоловый красный, БФС [2].
В основе ещё одной группы количественных методов лежит способность белковых растворов менять цвет раствора индикатора при их смешивании. Для этого используется индикатор БФС, в растворе с pH <5 он находится преимущественно в катионной форме, имеющей жёлтую окраску. При добавлении в раствор белков, способных связываться с БФС, происходит связывание индикатора и изменение соотношения между катионной и анионной формами индикатора в пользу последней. Это сопровождается изменением окраски на синюю. Большинство белков связываются с pH <5, но для белков Бенс-Джонса и глобулинов необходимо изменение pH до 3,0 или ниже. Хотя даже с этим изменением чувствительность для альбумина остаётся более высокой для альбумина, чем для других белков.
Также широко применяется метод разделения белков мочи на фракции и их дальнейшее определение. Разделение белков мочи начинается с её концентрирования, после чего их разделяют с помощью электрофореза на различных носителях — полиакриламидный гель, агароза, ацетат-целлюлозная мембрана. Для концентрирования используют растворы полимеров, поливинилпирролидона, полиэтиленгликоля, гуммиарабика, желатины и метод ультрафильтрации. Однако следует учитывать, что при этом может нарушиться исходный белковый спектр.
По характеру спектров электрофореграммы мочи можно разделить на две группы:
1) Напоминает электрофореграмму сыворотки крови; наблюдается при попадании в мочу многих белков плазмы крови; идентификация отдельных белковых фракций не представляет трудностей.
2) Меньшее количество фракций, расположение может совпадать с соответствующими зонами электрофореграммами сыворотки крови. Подобный тип обнаруживают при протеинуриях, связанных с воспалительными и деструктивными процессами в канальцах.
Электрофорез в присутствии детергента додецилсульфата натрия позволяет выявить до 100 различных белков, при усложнении процедуры, это число увеличивается до 200 [2]. При множественной миеломе продуцируются моноклональные иммуноглобулины, целые молекулы которых структурно не отличаются от нормальных и на электрофореграмме образуют интенсивную узкую полосу в зоне миграции γ-глобулинов — так называемый М-градиент. Обнаружение М-градиента свидетельствует об однородности физико-химических свойств парапротеинов, в отличие от нормальных иммуноглобулинов. Белок Бенс-Джонса представляет собой гомогенную популяцию каппа- и лямбда-цепей молекулы иммуноглобулинов. Размеры пор в клубочках ограничивают фильтрацию белков с ММ более 30 кДа. Каппа-цепи чаще всего присутствуют в виде мономеров с массой 25 кДа, из-за этого они фильтруются гораздо быстрее лямбда-цепей, которые являются димерами. В связи с этим, в сыворотке крови обнаруживается большее количество λ-цепей. При электрофорезе белков сыворотки крови М-градиент может встречаться у пожилых людей без опухоли, однако обнаружение белка Бенс-Джонса практически безошибочно указывает на злокачественную природу заболевания. Отсюда следует вывод, что в сыворотке и моче пациентов следует определять следующие показатели:
— Наличие парапротеинов на электрофореграмме;
— Количественное определение белка в М-градиенте;
— Выявление типа моноклонального иммуноглобулина;
— Определение концентрации белка в моче;
— Качественная характеристика белковых фракций с помощью электрофореграммы.
В настоящее время при подозрении на множественную миелому у пациента используются иммуногистохимическое или иммунофлуоресцентное исследование. В результате, в зависимости от типа секреции, в цилиндрах обнаруживают фиксацию каппа или лямбда типа лёгких цепей.
Анализ крови и биоптата
Для достоверного установления диагноза множественной миеломы необходимо провести оценку инфильтрации костного мозга плазматическими клетками. Стандартными методами для этого являются аспирация и биопсия. Дополнительными методами являются определение уровня гемоглобина в развернутой формуле крови, уровня креатинина и кальция сыворотки крови по классификации CRAB. При оценке клинического анализа крови больного ММ обращает на себя внимание высокие показатели СОЭ и анемия. Анемия чаще нормохромная, нормоцитарная с низким содержанием ретикулоцитов в крови. Гораздо реже у больных ММ может быть выявлена тромбоцитопения, лейкопения и нейтропения. Возможно выявление единичных плазматических клеток и крайне редко — плазмобластов. Именно высокая СОЭ у 70% больных является основанием для комплексного обследования больного ММ и часто опережает клинические симптомы заболевания. Обычно у больных ММ выявляется увеличение в сыворотке крови IgG >35 г/л, IgA >20 г/л и/или увеличение κ или λ легких цепей в суточной порции мочи более 1 г, но большую диагностическую значимость имеет доказательство моноклональности патологического белка. При исследовании биохимических показателей крови выявляется увеличение общего белка за счет глобулиновой фракции (часто в сочетании с гипоальбуминемией) и появление М-компонента на электрофореграмме белков. При поражении почек у больных ММ выявляется увеличение уровня креатинина. Уровень мочевой кислоты в сыворотке крови повышается в активной фазе заболевания, а также на фоне лечения. При исследовании электролитов часто выявляется гиперкальциемия, гиперфосфатемия, гипонатриемия, гипо- или гиперкалиемия. Изменения в коагулограмме обычно обусловлены нарушениями белковосинтетической функции печени и выраженным увеличением моноклонального белка в сыворотке крови с развитием синдрома гипервязкости. В этом случае наблюдается гипокоагуляция. В активной фазе заболевания у больных ММ отмечается увеличение уровня С-РБ, β2-микроглобулина, интерлейкина 6, лактатдегидрогеназы в сыворотке крови. Величина этих показателей ассоциирована с опухолевой массой и может быть использована для стадирования заболевания и оценки эффективности лечения. [3]
Отдельно следует остановиться на цитогенетических методах исследования при ММ. Хотя множественная миелома — клональное заболевание, хромосомные нарушения при использовании стандартных методов цитогенетического исследования выявляются только у 20-60% больных на ранних этапах заболевания и у 50-90% больных с III стадией заболевания. Наибольшую информативность имеет метод флюоресцентной in situ гибридизации (FISH) c флюоресцентным окрашиванием цитоплазматических иммуноглобулинов (cIg FISH или FICTION), который выявляет аномалии в 89% случаев. Специфические изменения кариотипа включают количественные и структурные нарушения кариотипа. Наиболее часто у больных ММ выявляется моносомия 13 хромосомы (или потеря части 13 хромосомы), более редко – моносомия 14, 8 хромосом и трисомия или тетрасомия 9 хромосомы, более редко – 3, 19, 15, 11, 7, 5, 18, 21 хромосом. Структурные изменения хромосомного аппарата у больных ММ схожи с изменениями при других лимфопролиферативных заболеваниях. Изменения в области региона 14q (switch-регион Н-цепи Ig) связаны с транслокациями t(11;14)(q13;q32), t(8;14)(q24;q32), t(14;18)(q32;q21); изменения в области региона 16p или 16q – c транслокациями 21t(1;16)(p11;p11), t(1;16)(p10;p10). Кроме того, возможны структурные изменения в области 1p или 1q (частичная делеция, трисомия), 19q13 или 19р13, 6q, 17q, 17p,2p12, 22q11, 7q. Цитогенетическое исследование при ММ имеет принципиальное значение, так как позволяет формировать группу риска и выбирать оптимальный подход к лечению. Кроме того, цитогенетическое исследование и FISH используются для диагностики и лечения резидуальной болезни у больных ММ. Также следует сказать о новейших перспективных разработках в области диагностики множественной миеломы. Одним из таких методов является исследование циркулирующей микроРНК в сыворотке крови. Так, уровни miR-34a и let-7e могут определить состояние множественной миеломы с чувствительностью 80.6% и специфичностью 86.7%. Что касается моноклональной гаммапатии, то здесь чувствительность составила 91.1% и специфичность на уровне 96.7%. [6]
Глава 5
Ведение пациентов с ММ
Тактика ведения больных моложе 65 лет и пожилых больных отличается. Для лечения первичных пациентов ММ моложе 65 лет без серьезной сопутствующей патологии используют высокодозную химиотерапию (ВХТ) с трансплантацией аутологичных гемопоэтических стволовых клеток (ауто-ТГСК). Больным старше 65 лет или молодым больным с тяжелыми сопутствующими заболеваниями следует рекомендовать комбинации на основе новых лекарственных препаратов без ВХТ с трансплантацией аутологичных ГСК. [3]
Не кандидаты на высокодозную химиотерапию с трансплантацией
аутологичных ГСК (пожилые больные).
В настоящее время для лечения пожилых больных с впервые выявленной ММ следует использовать программы с включением нового лекарственного препарата бортезомиба.
Комбинация бендамустина (рибомустина) с преднизолоном (схема BP) недавно введена в арсенал лечения больных с впервые диагностированной ММ старше 65 лет, не являющихся кандидатами для проведения ВХТ, с клиническими проявлениями нейропатии, препятствующей использованию терапии с включением талидомида и бортезомиба.
В других странах для лечения пожилых больных с впервые диагностированной ММ используют сочетание талидомида с мелфаланом и преднизолоном (схема MPT), программы на основе леналидомида: леналидомид с дексаметазоном в низкой дозе (схема Rd), сочетание леналидомида с мелфаланом и преднизолоном (схема MPR). Лечение по схеме MPR с последующей поддерживающей терапией леналидомидом превосходит по эффективности химиотерапию МP.
Кандидаты на высокодозную химиотерапию с последующей трансплантацией
аутологичных(собственных) ГСК
Больные в возрасте до 60-65 лет, которым впервые установлен диагноз ММ, исходно могут рассматриваться в качестве кандидатов на высокодозную консолидацию, включающую одну или две трансплантации аутологичных стволовых гемопоэтических клеток. Возрастные ограничения обусловлены тем, что у пожилых больных возрастает риск трансплантант-ассоциированной летальности.
I этап лечения: индукция.
В настоящее время наиболее распространенными схемами индукционной терапии являются VD (бортезомиб +дексаметазон), PAD (велкейд, адриабластин и дексаметазон) и VCD (бортезомиб +циклофосфамид+дексаметазон). С учетом планируемой аутологичной трансплантации, представляется целесообразным начинать индукционную терапию со схем, включающих 3 препарата — PAD, VCD, поскольку клиническими исследованиями было показано, что эти трехкомпонентные схемы обладают более высокой эффективностью, чем VD. Согласно рекомендациям NCCN, в качестве схем индукционной терапии также можно рассматривать высокие дозы дексаметазона или же сочетание липосомального доксорубицина, винкристина и дексаметазона.
Количество курсов индукционной терапии определяется противоопухолевым ответом на лечение, а также центром, где в дальнейшем будет проводиться высокодозный этап лечения.
II этап лечения: трансплантация
· Мобилизация гемопоэтических стволовых клеток крови
Целью мобилизации является заготовка достаточного количества CD34+ клеток для выполнения двух аутоТГСК. Мобилизацию ГСК целесообразно выполнять максимально рано после завершения индукционной терапии (интервал от завершения последнего идукционного курса до введения циклофосфамида — не более 4 нед).
Наиболее часто используемым режимом мобилизации является сочетание химиотерапевтических препаратов (циклофосфана в дозе 2-4 г/м2, вепезида, цитозара, курсов DPACE, CAD, VD-PACE, DHAP и др) и гранулоцитарного колоние-стимулирующего фактора (Г-КСФ).
· Предтрансплантационное кондиционирование с последующей трансфузией аутологичных гемопоэтических стволовых клеток.
Наиболее предпочтительный режим кондиционирования включает в себя высокие дозы мелфалана (200 мг/м2).
III этап лечения: консолидация
Целью консолидирующей терапии является повышение качества противоопухолевого ответа, достигнутого на предыдущих этапах лечения. Консолидирующая терапия включает в себя ограниченное число курсов препаратами в полных дозах (например, VCD, VD).
IV этап: поддерживающая терапия
Поддерживающая терапия направлена на подавление пролиферации остаточного клона опухолевых клеток и выполняется с целью предупреждения рецидива заболевания. В настоящее время рядом крупных многоцентровых исследований показано значение поддерживающей терапии, назначаемой как после аутологичной трансплантации, так и после стандартной индукционной терапии. При этом в качестве терапевтических препаратов рассматриваются леналидомид (в дозе 10-15 мг/сут до прогрессии) и бортезомиб (в дозе 1,3 мг/м2 каждые 2 недели в течение 2-х лет или до прогрессии).
Контрольное обследование
После аутотрансплантации контрольное обследование выполняется через 60 дней после переливания аутологичных ГСК. Оцениваются показатели общего анализа крови (с подсчетом лейкоцитарной формулы и количества тромбоцитов), биохимического анализа крови (мочевина, креатинин, кальций), выполняется иммунохимическое исследование крови и мочи с количественным определением М-протеина и белка Бенс-Джонса, показателей поликлональных иммуноглобулинов, выполняется иммунофиксация. Рентгенологические исследования (рентгенография, МРТ, КТ), исследование аспирата и/или биоптата костного мозга, исследование свободных легких цепей выполняется по показаниям. В дальнейшем контрольные обследования осуществляются с частотой 1 раз в 3 месяца. Поддерживающую терапию целесообразно начинать после полноценного восстановления гемопоэза, когда в гемограмме число лейкоцитов стойко превышает 2,5 х 109/л, а число тромбоцитов — 100 х 109/л.

