Яблоки традиционно относятся к основным видам сырья для производства сидра. Благодаря высокому содержанию сахаров, органических кислот, дубильных веществ, витаминов, микроэлементов яблочный сок является оптимальным сырьём для производства сброженных напитков. В условиях стабильного роста интереса потребителей к традиционным русским напиткам, таким как квас, сидр, медовуха, актуальной задачей является исследование факторов, влияющих на технологию и показатели качества готового продукта. Важнейшим критерием, определяющим пригодность плодового сырья для использования в производстве сидра, является содержание дубильных веществ, в том числе танина.
Цель работы – апробация методик и последующее сравнение результатов спектрофотометрического и перманганатометрического определения содержания танинов в растительном сырье для такого объекта исследования как яблочный сок.
Спектрофотометрическое определение основано на образовании окрашенных в жёлтый цвет соединений при взаимодействии водного раствора танина с раствором молибдата аммония в кислой среде. Стандартный водный раствор танина был приготовлен из точной навески с последующим растворением и доведением до метки дистиллированной водой в мерной колбе на 100 мл. Затем аликвотная часть данного раствора объёмом 5 мл и 10 мл 2 % раствора молибдата аммония были количественно перенесены в другую мерную колбу вместимостью 100 мл и доведены до метки дистиллированной водой. Концентрация танина в приготовленном таким образом стандартном окрашенном растворе составила 4,8900·10–5 г/мл. Определение оптической плотности осуществлялось при длине волны 395±2 нм в соответствии со значением максимума на полученной нами спектральной характеристике для стандартного окрашенного раствора танина (рисунок). Это даёт возможность использовать длину волны 395±2 нм в качестве аналитической для методики количественного определения танина. В качестве раствора сравнения был приготовлен раствор, состоящий из того же объёма стандартного раствора танина без добавления молибдата аммония, доведенного до метки дистиллированной водой в мерной колбе на 100 мл.
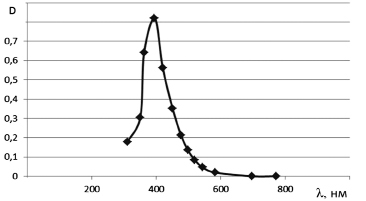
Спектральная характеристика стандартного раствора танина
Были использованы кюветы с толщиной поглощающего слоя 20 мм для получения спектральной характеристики и 10 мм для дальнейшего измерения оптической плотности стандартного окрашенного раствора танина.
В мерную колбу объемом 100 мл вносили 5 мл отфильтрованного исследуемого сока, 10 мл 2 % раствора молибдата аммония, доводили до метки дистиллированной водой. Через 15 минут измеряли оптическую плотность полученного окрашенного раствора в тех же условиях: при длине волны 395 нм в кювете с толщиной поглощающего слоя 10 мм. В качестве раствора сравнения (с целью исключения влияния на оптическую плотность собственной окраски сока) использовали раствор, состоящий из 5 мл того же сока и дистиллированной воды, доведённой до метки в мерной колбе вместимостью 100 мл.
Содержание танинов (в г на 100 г яблок, или в массовых долях) рассчитывали по формуле
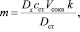
где Dx – оптическая плотность раствора, составленного из исследуемой аликвотной части яблочного сока с молибдатом аммония и водой; сст – концентрация стандартного окрашенного раствора танина, г/мл; Vсока – объём сока, полученный из 100 г яблок, мл; Dст – оптическая плотность стандартного окрашенного раствора танина, измеренная при толщине поглощающего слоя 10 мм, которая составила 0,501; k – коэффициент, учитывающий разбавление.
Результаты анализа представлены в табл. 1.
Таблица 1
Содержание танинов в различных сортах яблок по данным спектрофотометрии
|
Сорт яблок |
Объём сока, полученный из 100 г яблок, мл |
Оптическая плотность D |
Масса танинов, мг/100 г яблок |
Массовая доля танинов ω % |
|
Призовое |
63,3 |
0,247 |
320 |
0,032 |
|
Лигол |
63,1 |
0,448 |
579 |
0,0579 |
|
Россошанское полосатое |
60,4 |
0,329 |
407 |
0,0407 |
|
Острогожское |
58,8 |
0,194 |
234 |
0,0234 |
Полученные результаты по порядку величины хорошо согласуются с данными по содержанию танинов в яблочном соке, представленными в работах [1–3].
Перманганатометрическое определение основано на лёгкой окисляемости танина перманганатом калия в присутствии кислого раствора индигокармина при комнатной температуре. В качестве титранта использовали стандартизированный по щавелевой кислоте 0,009535 н. раствор перманганата калия. Для приготовления раствора индигокармина 1 г его растворяли в 50 мл концентрированной серной кислоты, затем разбавляли дистиллированной водой в мерной колбе вместимостью 1 л.
В титровальную колбу помещали 2,50 мл раствора индигокармина, 2,50 мл исследуемого сока, доводили до метки дистиллированной водой до 150 мл. Титровали при постоянном перемешивании с помощью магнитной мешалки раствором перманганата калия. Наблюдали переход цвета раствора от синего (через бирюзовый) до жёлтого. Титрование заканчивали при появлении золотисто-жёлтого окрашивания.
Параллельно проводили контрольный опыт. В титровальную колбу помещали 2,50 мл раствора индигокармина, 2,50 мл стандартного раствора танина приготовленного из точной навески 0,1027 г в 100 мл воды, доводили до метки дистиллированной водой до 150 мл. Титровали при постоянном перемешивании с помощью магнитной мешалки раствором перманганата калия также до появления золотисто-жёлтого окрашивания. В результате 1 мл стандартизированного раствора перманганата калия окисляет 0,000201373 г дубильных веществ в пересчете на танин. Титрование проводили до получения трёх сходящихся результатов, отличающихся не более чем на 0,05 мл. Из трёх сходящихся результатов рассчитывали среднее арифметическое значение объёма титранта, пошедшего на титрование. Содержание танинов (в г на 100 г яблок, или в массовых долях) рассчитывали по формуле:
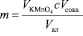 ,
,
где VKMnO4 – среднее арифметическое значение объёма стандартизированного раствора перманганата калия, пошедшего на титрование, мл; с – содержание танина, полученное в контрольном опыте, соответствующее 1мл 0,009535 н. раствора KMnO4, г/мл; Vсока – объём сока, полученный из 100 г яблок, мл; Vал – аликвотная часть исследуемого сока, мл.
Результаты анализа представлены в табл. 2.
Таблица 2
Содержание танинов в различных сортах яблок по данным перманганатометрии
|
Сорт яблок |
Объём сока, полученный из 100 г яблок, мл |
Объем титранта VKMnO4, мл |
Масса танинов, мг/100 г яблок |
Массовая доля танинов ω % |
|
1. Призовое |
63,3 |
7,50 |
382,4 |
0,03824 |
|
2. Лигол |
63,1 |
11,55 |
587,0 |
0,05870 |
|
3. Россошанское полосатое |
60,4 |
8,50 |
413,5 |
0,04135 |
|
4. Острогожское |
58,8 |
6,30 |
298,3 |
0,02983 |
Метод перманганатометрии рекомендован Государственной фармакопеей 11-го издания (ГФ XI) [4] как основной метод определения дубильных веществ. Однако он имеет ряд недостатков. Во-первых, нечёткий переход окраски титруемого раствора не позволяет объективно оценить точный момент изменения окраски, соответствующий конечной точке титрования. Поэтому при использовании перманганатометрии очень сильно проявляется субъективность исследователя. Во-вторых, имеет место окисление перманганатом калия не только дубильных, но и других сопутствующих веществ [5], чем, собственно, и объясняются завышенные, по сравнению с СФ-измерениями, результаты титриметрического анализа.
Определение методом спектрофотометрии исключает наличие субъективных ошибок, поскольку в его основе лежит измерение оптической плотности раствора при определенной длине волны, то есть используются физические характеристики раствора. Но у СФ-метода также имеется недостаток. Поскольку разные виды дубильных веществ имеют разные максимумы поглощения [6], возникает необходимость предварительного получения спектральных характеристик при использовании различных стандартных растворов. Но, поскольку максимумы поглощения находятся в довольно небольшом диапазоне длин волн, отвечающем фиолетовому участку спектра, на абсолютном суммарном содержании танинов такой небольшой разброс не сказывается. Поэтому, на наш взгляд, метод спектрофотометрии является более объективным, чем результаты методики перманганатометрии. В соответствии с полученными данными среди рассматриваемых сортов наибольшее значение содержания танина отмечено в яблоках сортов «Лигол» и «Россошанское полосатое» 579 и 407 мг/100 г яблок соответственно, что позволяет рекомендовать указанные сорта яблок для производства сидра [7–9].
Библиографическая ссылка
Колтышева О.Ю., Соколова С.А., Дьяконова О.В., Колобаева А.А., Котик О.А. СРАВНЕНИЕ РЕЗУЛЬТАТОВ СПЕКТРОФОТОМЕТРИЧЕСКОГО И ПЕРМАНГАНАТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ТАНИНОВ В ЯБЛОЧНОМ СОКЕ ДЛЯ ПРОИЗВОДСТВА СИДРА // Международный студенческий научный вестник. 2018. № 3-2. ;URL: https://eduherald.ru/ru/article/view?id=18249 (дата обращения: 05.04.2025).

