Злоупотребление алкоголем вследствие широкого распространения представляет серьезную медицинскую и социальную проблему. Пролонгированный прием алкоголя оказывает негативное влияние на все компартменты организма, однако печень наиболее подвержена его влиянию, поскольку именно в данном органе, происходит микросомальное окисление этанола. Для обозначения многочисленных модификаций в печени, связанных с алкоголем используется термин «алкогольная болезнь печени» (АБП) [1].
Алкогольная болезнь является актуальной проблемой на сегодняшний день. Систематический прием алкоголя — повышенный фактор риска возникновения и тяжелого течения хронических диффузных заболеваний печени, а также одна из причин ранней инвалидизации молодого и трудоспособного населения [2]. В настоящее время установлено пороговое ежедневное количество и продолжительность потребления алкоголя, приводящее к развитию АБП. Ежедневное потребление алкоголя в течение 10—12 лет в дозах, превышающих 40—80 г/сут для мужчин и 20—40 г/сут для женщин, может служить причиной алкогольного стеатоза/гепатита/цирроза [1]. Риск развития АБП сопряжен с гораздо меньшей дозой, а именно с употреблением 30 г этанола в сутки [3]. Исследования показали, что даже при умеренном употреблении алкоголя (≤10 г в день) формируется стеатоз печени [4].
АБП проявляется тремя основными клинико-морфологическими формами – алкогольным стеатозом, составляющим 60-90% случаев АБП, алкогольным гепатитом, наблюдающимся в 10-30% случаев и алкогольным циррозом печени в 8-20% случаев.
Клинические формы АБП могут встречаться как изолированно, так и в сочетании друг с другом. Эволюция АБП представлена на рисунке 1.
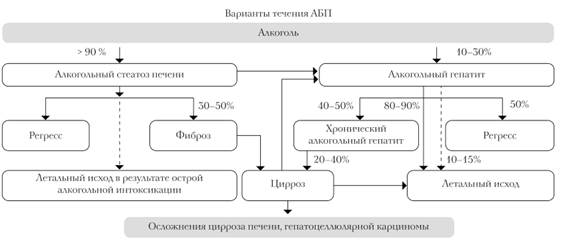
Рис. 1. Эволюция алкогольной болезни печени (Е. Kuntz, H-D. Kuntz, 2002 г.)
Алкогольный стеатоз (АС) – наиболее частая форма АБП. В изолированном виде выявляется, по разным данным у 50-90% больных, злоупотребляющих алкоголем [5]. Накоплены убедительные данные, свидетельствующие о том, что наличие высокого индекса массы тела (ИМТ), инсулинорезистентность представляют собой факторы прогрессирования стеатоза и стеатогепатита печени алкогольного генеза [6]. АС характеризуется диффузным патологическим внутри- и внеклеточным отложением капель нейтрального жира. Стеатоз может формироваться за короткий период (около 3-4 недель), подвергаться регрессу в течение нескольких недель или месяцев, либо трансформироваться в гепатит, фиброз и алкогольный цирроз печени [5].
У пациентов с циррозом печени признаки алкогольной зависимости выявляются значительно чаще по сравнению с пациентами, болеющими стеатозом и гепатитом, что говорит о несомненном влиянии алкогольной зависимости на развитие цирроза печени уже в течение 9 месяцев [7]. На этой стадии болезнь имеет неблагоприятный прогноз, даже если пациенты осознают, что алкоголь является причиной ухудшения качества их жизни [8].
Субъективная симптоматика при АС отмечается в 60-80% случаев и носит неспецифический характер. Больных беспокоит повышенная утомляемость, снижение аппетита, метеоризм, ощущение тяжести в правом подреберье и эпигастральной области и диарея после употребления пищи, содержащей большое количество жиров. Обычно появление указанных симптомов связано с недавним употреблением больших доз алкоголя. Объективная симптоматика поражения печени (пальмарная эритема, умеренная гепатомегалия, телеангиоэктазии) определяется у 10-30% больных. Желтуха и спленомегалия встречаются редко [5].
В патогенезе алкогольиндуцированного стеатоза можно выделить несколько факторов (рис. 2).
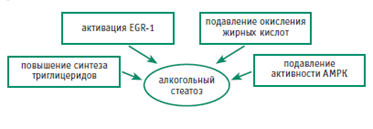
Рис.2. Этиопатогенетические факторы алкогольного стеатоза. Примечание. AMPK — аденозинмонофосфат-активируемая протеинкиназа (AMP-activated proteinkinase); EGR-1 — фактор транскрипции (early growth response).
Во-первых, под влиянием этанола происходит повышение синтеза триглицеридов. Стимуляция липогенеза происходит за счет воздействия на факторы транскрипции, которые стимулируют липогенез и тормозят окисление жирных кислот. Таким фактором является белок SREBP-1c (sterol regulatory element-binding protein 1c), активирующий липогенные гены. Продукт метаболизма алкоголя ацетальдегид способствует транскрипции гена SREB-1с непосредственно, либо опосредованно — через аденозин и каннабиноиды. В результате повышается уровень липогенных энзимов. Таким образом, этанол преображает печень из «жиросжигающего» в «жиронакопляющий» орган.
Во-вторых, этанол подавляет β - окисление жирных кислот в гепатоцитах путем инактивации рецепторов, активируемых пероксисомными пролифераторами (PРAR-α) и вовлеченных в регуляцию транспортировки и их окисления. Следует отметить, что этанол-индуцированное подавление цикла Кноопа-Линена — обратимый процесс: в экспериментальных исследованиях крысам одновременно давали этанол и агонисты PPAR-α, индукция PPAR-α, ускорявшая окисление жирных кислот, одновременно предотвращала жировую инфильтрацию печени [9].
Жировая инфильтрация гепатоцитов, преимущественно крупнокапельная, выявляется у 60-100% лиц, употребляющих этанол в гепатотоксических дозах. Стеатоз является обратимой стадией АБП при условии прекращения приема алкоголя у генетически предрасположенных к данному заболеванию лиц [9]. АС печени, обычно протекающий бессимптомно, может быть полностью обратим при отказе от алкоголя примерно через 4–6 недель. Некоторые исследования показали, что прогрессирование фиброза и исход в цирроз происходит у 5–15% пациентов, несмотря даже на полную абстиненцию [10].
Еще одним важным «игроком» в алкогольиндуцированном стеатозе является фактор транскрипции EGR-1 (early growth response 1). Он активируется под влиянием пептидов (васкулоэндотелиальный фактор роста - VEGF-A). Гены, имеющие отношение к алкогольному поражению печени, имеют промоутерные регионы, которые связывают EGR-1. Среди этих генов имеются те, которые кодируют тромбоцитарный фактор роста (platelet-derived growth factor — PDGF), трансформирующий фактор роста бета (transforming growth factor beta — TGF -β), молекулы межклеточной адгезии 1 (intercellular adhesion molecule 1 — ICAM-1), ФНО-α. ФНО-α является липогенным цитокином, вызывающим активацию SREBP-1с и повышающим биосинтез липидов
Алкоголь увеличивает отношение никотинамидадениндинуклеотид восстановленный/окисленный (НАД/НАДН), нарушая β-окисление жирных кислот в митохондриях и подавляя эндогенный синтез глюкозы из неуглеводных компонентов, что может приводить к стеатозу.
Таким образом, алкогольный стеатоз представляет собой результат дисбаланса в липидном обмене. Основными событиями являются усиление липогенеза путем активации липогенных генов и подавление окисления жирных кислот в печени, и алкоголь выступает в роли индуцирующего (триггерного) фактора [11].
Механизм трансформации стеатоза в стеатогепатит включает несколько патогенетических звеньев, которые являются идентичными как при неалкогольном, так и алкогольном поражениях печени. В процессе накопления свободных жирных кислот (СЖК) гепатоцит становится более уязвимым и чувствительным к токсическим воздействиям. СЖК, которые поступают из кишечника или синтезируются в печени, участвуют в образовании триглицеридов. Триацилглицериды в последующем преобразовываются в атерогенные формы липопротеинов очень низкой плотности [12].
Чрезвычайно важна ранняя диагностика алкогольного стеатоза. Необходимым этапом является правильный сбор анамнеза с использованием специальных опросников и тщательный осмотр пациента (увеличение околоушных слюнных желез, расширение сосудов кожи щек и носа, склер, атрофия мышц плечевого пояса, пальмарная эритема, гинекомастия, полинейропатия, контрактура Дюпюитрена, хронический панкреатит, признаки поражения сердца, нефропатия) [13].
Показатели функционально-печеночных тестов при АС не изменены, либо характеризуются умеренным транзиторным повышением активности аминотрансфераз и сывороточных маркеров холестаза – γ- глутамилтранспептидазы (ГГТП), щелочной фосфатазы (ЩФ), конъюгированного (нетоксичного) билирубина и липидов [5].
У 70% госпитализированных пациентов со стеатозом выявляется увеличение печени, а у одной трети из них наблюдаются изменения биохимических маркеров. Уровень аспарагиновой трансаминазы (АСТ) и аланиновой трансаминазы (АЛТ) редко превышает 300 Ед/мл. У пациентов с АБП коэффициент де Ритиса часто превышает 2. Уровень АСТ и АЛТ, превышающих 300 Ед/мл у пациента, злоупотребляющего алкоголем, позволяет предположить наличие повреждения гепатоцитов другой этиологии.
АБП характеризуется умеренно выраженным цитолитическим и иммуновоспалительным синдромом при отсутствии признаков цирротической трансформации печени. Значительно повышается уровень иммуноглобулина A (IgA), который откладывается в стенке печеночных синусоидов и/или почечных эндотелиоцитах. Проявлением клеточных механизмов печеночного поражения служит увеличение числа цитотоксических лимфоцитов наряду с повышенной экспрессией на мембранах молекул главного комплекса гистосовместимости I и II классов [13].
В последние годы в качестве нового предиктора алкогольной интоксикации предложен безуглеводистый (десиализированный) трансферрин, повышение концентрации которого в крови происходит при регулярном приеме 60 г и более этанола в сутки [14].
Уровни ЩФ часто находятся в пределах нормы или незначительно повышены, а уровни ГГТП обычно увеличиваются, независимо от наличия болезни печени, у больных, злоупотребляющих алкоголем. Специфичность ГГТП ограничена, так как большинство лекарственных средств вызывают повышение активности данного фермента.
Тесты, отражающие состояние функции печени: сывороточный альбумин, билирубин и протромбиновое время (протромбиновый индекс) обычно изменяются только при выраженном повреждении печени.
Гематологические показатели: количество тромбоцитов колеблется в пределах нормы с тенденцией к снижению, макроцитарная анемия, количество лейкоцитов обычно повышено (при алкогольном гепатите возможны лейкемоидные реакции).
Хроническое злоупотребление алкоголем сопровождается: гиперурикемией, гипертриглицеридемией, гипомагниемией, гипокалиемией и увеличением корпускулярного объема эритроцита (MCV).
Наличие карбогидратного трансферрина может быть специфичным признаком при АБП, но чувствительность теста недостаточно высока, что ограничивает его использование для диагностики хронического алкоголизма [1].
В последнее время особое внимание уделяется методам верификации стеатоза печени, которые можно разделить на инвазивные, малоинвазивные и неинвазивные.
Количественное определение степени стеатоза печени и фиброза печени проводится с использованием трех традиционных методик: биопсия, непрямая эластометрия, лабораторные индексы. Проведение данных исследований позволяет оценить морфологические изменения структуры печени, оценить тяжесть фиброза печени и воспалительных изменений, возможные сопутствующие поражения, сформулировать окончательный диагноз. На основании полученных данных принимается решение об объеме проводимого лечения (Рис.3) [15].
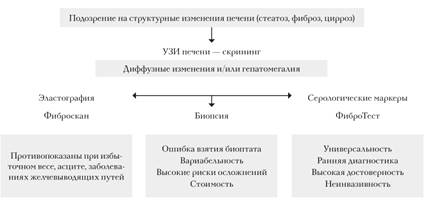
Рис.3. Тактика выбора метода уточнения структурных нарушений (фиброз, цирроз). (С.С.Вялов, 2011г.)
К неинвазивным методам относятся: УЗИ, КТ, МРТ, эластометрия (Фиброскан). Выделяют несколько ультразвуковых признаков стеатоза печени: дистальное затухание эхосигнала, диффузная гиперэхогенность печени («яркая печень»), увеличение эхогенности печени по сравнению с почками, обеднение сосудистого рисунка. УЗИ может служить единственным методом, необходимым для распознавания стеатоза печени при отсутствии у пациента клинической симптоматики и выявлении отклонений функциональных печеночных тестов, а также при невозможности проведения гистологического исследования ткани печени. По данным ультразвукового исследования можно с большой вероятностью определить наличие выраженного стеатоза печени и по вычислению индекса затухания эхосигнала определить его степень [16].
Картина стеатоза печени на УЗИ может наблюдаться при целом ряде заболеваний, имеющих разную этиологию, прогноз и требующих разных подходов в лечении (хронические вирусные гепатиты, алкогольный гепатит, обменные заболевания печени и т. д.) [17].
Изменения, аналогичные ультразвуковым результатам, обнаруживаются при КТ и МРТ. С помощью протонной МР-спектроскопии проводится расчет процентной концентрации липидов в паренхиме печени. Если значение превышает 6,5 %, то наличие жировой инфильтрации печени считается подтвержденным [16].
Диагностику фиброзного процесса в паренхиме печени на ранних стадиях проводят при помощи комплексного эластометрического обследования пациентов. Теоретической предпосылкой для использования этого метода явился клинический опыт трактовки уплотнения печени при пальпации в пользу выраженного фиброза или цирроза печени [18].
Для диагностики фиброза печени применяются лабораторные неинвазивные методы (Fibrotest, Fibrometer Enhanced Liver Fibrosis панель, Hepascore), основанные на регистрации определенных маркеров сыворотки крови. Тест разработан во Франции известной французской компанией Biopdictive. В январе 2007 года министерство здравоохранения Франции признало ФиброТест реальной альтернативой инвазивным методам диагностики [4].
Hepascore включает определение уровня билирубина, ГГТП с учетом показателей обмена веществ внеклеточного матрикса (гиалуроновой кислоты, α2-макроглобулина), возраста и пола пациента. Enhanced Liver Fibrosis включает определение таких параметров, как гиалуроновая кислота, тканевой ингибитор металлопротеиназ-1, проколлаген [4].
В качестве маркера рассматривается концентрация гиалуроновой кислоты, которая коррелирует с гистологическим фиброзированием при прогрессировании АБП. При оценке прогноза АБП концентрация гиалуроновой кислоты в сыворотке крови может быть полезна в мониторировании фиброза печени, в уменьшении потребности в повторных биопсиях и при наличии противопоказаний к ним [19].
Тканевой ингибитор матрикса металлопротеиназы, пропептид коллагена III типа, матрикс металлопротеиназы, тенасцин, ламинин - другие сывороточные маркеры предрасположенности к фиброзу у пациентов с прецирротическим алкогольным поражением печени. [19].
Измерение ригидности печени (эластометрия) является надежным инструментом для оценки печеночного фиброза у больных с АБП. При предоставлении данных необходимо учитывать выраженность признаков цитолиза, холестаза, ИМТ, так как указанные параметры влияют на показатели ригидности печени. Чувствительность эластометрии составляет 80%, специфичность – 90%. [4].
Эластометрия печени проводится при помощи аппарата FibroScan. В основе использования данного прибора лежит закон Гука (реакция материала на сжатие). Механически FibroScan - удар штифта датчика наносится через межреберье по правой доле печени, после чего с помощью ультразвукового М- и А-режима оценивается скорость продвижения сдвиговой волны через стандартный 4-сантиметровый участок ткани печени. На основании 10 достоверных замеров рассчитывается эластичность печени в кРа в абсолютных цифровых значениях, что позволяет определить стадию фиброза (F0–4), и одновременно осуществляется замер САРТМ-функцией (Controlled Attenuation Parameter - позволяет количественно рассчитать снижение амплитуды ультразвуковых сигналов в печени), которая применяется для определения степени (или балльности S0–3) стеатоза печени [16].
Трансабдоминальное ультразвуковое исследование и транзиторная эластометрия не отражают изменения в паренхиме печени на ранних стадиях в труднодоступных сегментах печени, таких как 1, 2, 4, 5, 8, тем самым не дает возможности подтверждения злокачественной или доброкачественной патологии. У пациентов с узкими межреберными промежутками, с избыточной массой тела установление датчиков вызывает определенные трудности в получении правильного результата исследования.
«Золотым» стандартом диагностики заболеваний печени остается пункционная биопсия. Но этот метод обладает рядом недостатков – это инвазивность, противопоказания к проведению данной манипуляции, плохая переносимость пациентами, метод недостаточно чувствителен, так как объем исследуемой ткани составляет всего около 1/50000 органа, недостаточно обученный медицинский персонал в проведении биопсии печени, биоптат морфологи могут интерпретировать по-разному [20].
Стеатоз печени является важной медицинской и социальной проблемой, так как, несмотря на благоприятное течение, это заболевание может приводить к развитию воспалительных изменений в печени с исходом в цирроз. Пациентам с АБП необходимо значительно снизить или полностью отказаться от употребления алкоголя, соблюдать сбалансированную диету, изменить свой образ жизни.
Существует необходимость своевременной диагностики осложнений АБП, применение различных методов, для того чтобы поддерживать качество жизни больных, уменьшить частоту летальных исходов, предотвратить возникновение осложнений [1].
Библиографическая ссылка
Невзорова М.С., Чепкасова Н.И., Боталов Н.С. РОЛЬ КЛИНИКО-ЛАБОРАТОРНЫХ И ИНСТРУМЕНТАЛЬНЫХ МЕТОДОВ В ДИАГНОСТИКЕ АЛКОГОЛЬНОГО СТЕАТОЗА // Международный студенческий научный вестник. 2017. № 6. ;URL: https://eduherald.ru/ru/article/view?id=17990 (дата обращения: 07.04.2025).

