Постановка проблемы.
Гидроксид натрия, хлорид натрия, сульфат меди, как и многие другие вещества являются незаменимыми в химической промышленности. Постоянно ведутся разработки новых видов оборудования, используемого на химических производствах, ищутся и находятся новые технологические решения. Знание численных значений электрических и диэлектрических характеристик перечисленных и других веществ способно во многом упростить моделирование технологических процессов, происходящих на производствах с их использованием.
Цель исследования состоит в измерении удельного электрического сопротивления растворов ряда электролитов.
Практическая значимость работы обусловлена возможностью использования приведенных в работе экспериментально полученных данных в качестве справочного материала.
Обзор публикаций по теме исследования.
Актуальность исследования подтверждается публикациями на эту тему.
В статье [1] показано, что диэлектрические характеристики РЭ можно связать их с эквивалентной и удельной проводимостью. Например, выведена формула описывающая соотношение удельной электропроводности РЭ, его коэффициента диэлектрической проницаемости, вязкости растворителя и его температуры.
Диссертация [2] рассматривает электрические и диэлектрические свойства таких РЭ, как муравьиная и уксусная кислоты. Поднимается вопрос о практическом применении накопленной информации, выводятся общие уравнения для термодинамических расчетов РЭ, приводятся данные об электрической проводимости РЭ.
Статья [3] рассматривает вольт-амперные характеристики растворов хлоридов натрия и калия, полученных на установках различной конструкции, а именно, с помощью стационарной и импульсной схем.
Сотрудниками московского предприятия «Г-4665» Бухаровым, Герасимовым и Федоткиным был изобретен «Жидкостный резистор, содержащий заполненный электролитом герметичный полый корпус из изоляционного материала» [4]. Разработка представляет собой полый диэлектрический цилиндр, заполненный электролитом с двумя электродами, имеющий специальный отсек с воздушным карманом. Это позволяет оградить воздушную среду и среду РЭ так, что пузырь воздуха не касается электродов.
Томский НИИ Высоких напряжений имеет схожее изобретение [5]. Однако здесь на границе воздушного кармана и среды электролита свободно плавает поплавок с закрепленным на нем электродом, что, по мнению авторов изобретения, позволяет нивелировать влияние теплового расширения РЭ на электрические характеристики резистора.
Работа [6] посвящена выведению формул для вычисления таких величин как, динамический коэффициент диэлектрической проницаемости ε1(ω) и динамический коэффициент диэлектрических потерь ε2(ω). Их численные значения являются, соответственно действительной и мнимой частями комплексного значения коэффициента диэлектрической проницаемости ε(ω).
Методика измерения электрического сопротивления растворов электролитов.
В целях накопления практических данных о проводимости РЭ была собрана установка для получения их вольт-амперных характеристик. Действующее значение переменного напряжения в цепи было неизменным, равным 12.000 В.
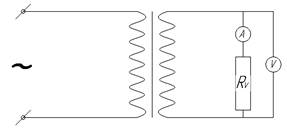
Рис. 1. Схема установки для измерения электрического сопротивления РЭ.
На рис. 1 изображена схема такой установки, здесь RV – сосуд для измерения электрического сопротивления растворов. Он представляет собой трубку из химически стойкого стекла ХС-2 (ГОСТ 21400-75) с двумя отливами, герметично закрытую с торцов резиновыми пробками с графитовыми электродами. Графит был выбран в качестве материала электродов из-за его химической инертности по отношению к исследуемым электролитам. Сопротивление графитовых электродов в растворе Rэл принимается за константу в данном эксперименте
Rэл = 24.446 Ом = const.
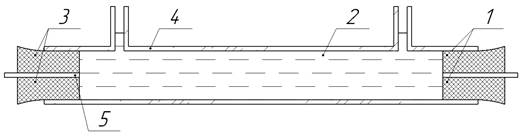
Рис. 2. Сосуд для измерения электрического сопротивления РЭ.
1, 3 – резиновые пробки, герметично прижатые к внутренним стенкам трубки,
2 – РЭ, 4 – стеклянная трубка с двумя отливами, 5 – графитовые электроды.
Сосуд для измерения электрического сопротивления электролитов представлен на рис. 2. Объем всех РЭ в сосуде V = 27.500 мл = const. При фиксированном значении действующего напряжения U = 12.000 В = const частотой f = 50.0 Гц = const проводились измерения протекающего через среду РЭ тока. Ток измерялся по четыре раза для каждого РЭ, дальнейшие вычисления проводили, используя среднее арифметическое значение тока для каждого РЭ. Сопротивление объема раствора вычислили по закону Ома для участка цепи, а удельное электрическое сопротивление [7; с. 258] приняли за электрическое сопротивление 1.000 мл РЭ.
Ввели через один из отливов в сосуд термопару (при этом объем раствора в сосуде не изменился), обмотали трубку проволокой из нихрома, подключили ее через ключ к источнику тока. Таким образом, получили возможность равномерно изменять температуру среды РЭ.
Работа проводилась с растворами гидроксида натрия (ч. д. а.), хлористого натрия (ч. д. а.), безводного сульфата меди (ч. д. а.), безводной уксусной кислоты (х. ч.) в бидистиллированной (мин. не более 7 мг/л) воде.
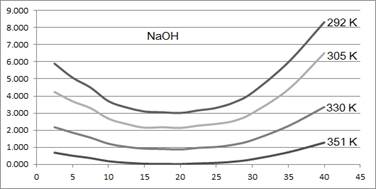
Рис. 3. Зависимость ρ(ω) для растворов NaOH при различных температурах. По вертикали ρ, Ом•см. По горизонтали ω, %.
Результаты измерений и вычислений. Перспективные направления исследований.
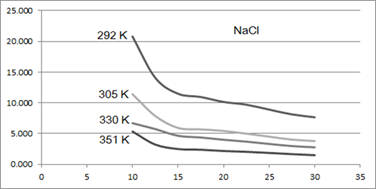
Рис. 4. Зависимость ρ(ω) для раствора NaCl при различных температурах. По вертикали ρ, Ом•см. По горизонтали ω, %.
Проведя все измерения и вычисления, составили таблицу их результатов (см. таблицу 1).
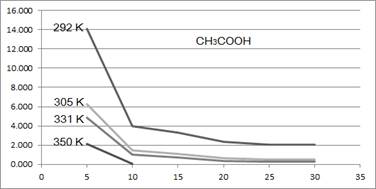
Рис. 5. Зависимость ρ(ω) для раствора CH3COOH при различных температурах. По вертикали ρ, Ом•см. По горизонтали ω, %.
На рисунках 3 – 6 представлены графики зависимости удельного электрического сопротивления растворов электролитов от их концентрации при различной температуре среды. По результатам измерений можно судить о пригодности исследуемых РЭ к использованию в качестве элементов электрических цепей переменного тока. Например, раствор NaOH (см. рис. 3) концентрацией 17,5 % по массе имеет наименьшее удельное сопротивление при температурах в диапазоне от 292 до 351 Кельвин. Растворы NaCl (см. рис. 4) и CH3COOH (см. рис. 5) концентрациями от 20 до 40 % по массе имеют относительно постоянное удельное электрическое сопротивление в диапазоне температур от 292 до 351 Кельвин. Это их свойство потенциально может быть использовано в технике, например, при использовании растворов этих электролитов в качестве активного элемента электрических цепей переменного тока. Эта тема заслуживает отдельного исследования.
Растворы же гидроксида натрия и сернокислой меди (см. рис. 6) могут гипотетически быть применены в качестве элемента прибора для измерения температуры из-за их относительно высокой чувствительности к ее изменениям в диапазоне концентраций от 2,5 до 30,0 % по массе.
Таблица 1.
Удельное электрическое сопротивление и удельная электропроводность водных растворов некоторых электролитов при различной температуре.
|
Т, К |
292.00 |
305.00 |
330.00 |
351.00 |
292.00 |
305.00 |
330.00 |
351.00 |
|
|
Электролит |
ω, % |
ρ, Ом∙см |
κ, Cм∙cм-1 |
||||||
|
NaOH |
2.5 |
5.896 |
4.234 |
2.172 |
0.685 |
0.170 |
0.236 |
0.460 |
1.460 |
|
5.0 |
5.075 |
3.690 |
1.854 |
0.505 |
0.197 |
0.271 |
0.540 |
1.982 |
|
|
7.5 |
4.498 |
3.291 |
1.564 |
0.367 |
0.222 |
0.304 |
0.639 |
2.724 |
|
|
10.0 |
3.698 |
2.672 |
1.209 |
0.183 |
0.270 |
0.374 |
0.827 |
5.468 |
|
|
12.5 |
3.331 |
2.363 |
1.024 |
0.093 |
0.300 |
0.423 |
0.977 |
10.765 |
|
|
15.0 |
3.095 |
2.148 |
0.917 |
0.035 |
0.323 |
0.466 |
1.090 |
28.643 |
|
|
17.5 |
3.051 |
2.173 |
0.900 |
0.027 |
0.328 |
0.460 |
1.112 |
36.908 |
|
|
20.0 |
3.008 |
2.133 |
0.871 |
0.016 |
0.332 |
0.469 |
1.148 |
60.624 |
|
|
22.5 |
3.162 |
2.269 |
0.968 |
0.055 |
0.316 |
0.441 |
1.033 |
18.086 |
|
|
25.0 |
3.306 |
2.368 |
1.020 |
0.086 |
0.302 |
0.422 |
0.980 |
11.643 |
|
|
27.5 |
3.636 |
2.548 |
1.160 |
0.161 |
0.275 |
0.393 |
0.862 |
6.201 |
|
|
30.0 |
4.196 |
3.000 |
1.420 |
0.297 |
0.238 |
0.333 |
0.704 |
3.370 |
|
|
35.0 |
5.977 |
4.387 |
2.244 |
0.707 |
0.167 |
0.228 |
0.446 |
1.414 |
|
|
40.0 |
8.324 |
6.509 |
3.357 |
1.272 |
0.120 |
0.154 |
0.298 |
0.786 |
|
|
NaCl |
2.5 |
− |
− |
− |
− |
− |
− |
− |
− |
|
5.0 |
437.208 |
218.160 |
218.160 |
108.635 |
0.002 |
0.005 |
0.005 |
0.009 |
|
|
7.5 |
37.644 |
19.215 |
15.056 |
10.671 |
0.027 |
0.052 |
0.066 |
0.094 |
|
|
10.0 |
20.781 |
11.410 |
6.696 |
5.345 |
0.048 |
0.088 |
0.149 |
0.187 |
|
|
12.5 |
14.078 |
7.865 |
5.739 |
3.217 |
0.071 |
0.127 |
0.174 |
0.311 |
|
|
15.0 |
11.484 |
5.925 |
4.643 |
2.494 |
0.087 |
0.169 |
0.215 |
0.401 |
|
|
17.5 |
10.949 |
5.688 |
4.372 |
2.377 |
0.091 |
0.176 |
0.229 |
0.421 |
|
|
20.0 |
10.149 |
5.439 |
4.004 |
2.173 |
0.099 |
0.184 |
0.250 |
0.460 |
|
|
22.5 |
9.699 |
4.993 |
3.692 |
2.034 |
0.103 |
0.200 |
0.271 |
0.492 |
|
|
25.0 |
8.906 |
4.504 |
3.321 |
1.854 |
0.112 |
0.222 |
0.301 |
0.539 |
|
|
27.5 |
8.122 |
4.026 |
2.973 |
1.658 |
0.123 |
0.248 |
0.336 |
0.603 |
|
|
30.0 |
7.656 |
3.794 |
2.773 |
1.487 |
0.131 |
0.264 |
0.361 |
0.673 |
|
|
CuSO4 |
2.5 |
3.730 |
2.190 |
1.542 |
0.601 |
0.268 |
0.457 |
0.648 |
1.664 |
|
5.0 |
3.607 |
2.100 |
1.476 |
0.558 |
0.277 |
0.476 |
0.677 |
1.793 |
|
|
7.5 |
3.331 |
1.925 |
1.332 |
0.472 |
0.300 |
0.520 |
0.751 |
2.117 |
|
|
10.0 |
3.140 |
1.816 |
1.240 |
0.410 |
0.319 |
0.551 |
0.806 |
2.438 |
|
|
12.5 |
3.031 |
1.724 |
1.174 |
0.375 |
0.330 |
0.580 |
0.852 |
2.664 |
|
|
15.0 |
2.989 |
1.757 |
1.148 |
0.358 |
0.335 |
0.569 |
0.871 |
2.792 |
|
|
17.5 |
3.052 |
1.738 |
1.185 |
0.382 |
0.328 |
0.575 |
0.844 |
2.616 |
|
|
20.0 |
2.871 |
1.575 |
1.102 |
0.332 |
0.348 |
0.635 |
0.907 |
3.010 |
|
|
22.5 |
2.411 |
1.311 |
0.848 |
0.176 |
0.415 |
0.763 |
1.179 |
5.697 |
|
|
25.0 |
3.095 |
1.724 |
1.207 |
0.402 |
0.323 |
0.580 |
0.828 |
2.485 |
|
|
27.5 |
3.667 |
2.149 |
1.509 |
0.581 |
0.273 |
0.465 |
0.663 |
1.722 |
|
|
30.0 |
3.896 |
2.301 |
1.630 |
0.655 |
0.257 |
0.435 |
0.614 |
1.527 |
|
|
CH3COOH |
5.0 |
14.078 |
6.238 |
4.867 |
2.104 |
0.071 |
0.160 |
0.205 |
0.475 |
|
10.0 |
3.967 |
1.424 |
0.979 |
0.082 |
0.252 |
0.702 |
1.022 |
12.160 |
|
|
15.0 |
3.331 |
1.121 |
0.734 |
− |
0.300 |
0.892 |
1.362 |
− |
|
|
20.0 |
2.334 |
0.646 |
0.350 |
− |
0.428 |
1.549 |
2.853 |
− |
|
|
25.0 |
2.049 |
0.510 |
0.241 |
− |
0.488 |
1.961 |
4.151 |
− |
|
|
30.0 |
2.049 |
0.510 |
0.241 |
− |
0.488 |
1.961 |
4.151 |
− |
|
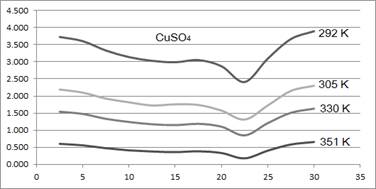
Рис. 6. Зависимость ρ(ω) для раствора CuSO4 при различных температурах. По вертикали ρ, Ом•см. По горизонтали ω, %.
Таким же образом могут быть использованы и растворы хлористого натрия и уксусной кислоты в концентрациями 2,5 – 7,5 % по массе (см. таблицу 1).
Растворы электролитов, изменяя свои электрические и диэлектрические характеристики под влиянием многих факторов, в том числе, температуры, давления среды, концентрации вещества в растворителе, частоты протекающего тока, могут быть применены во многих отраслях промышленности и сферах экономики в качестве датчиков и элементов измерительных приборов.
Библиографическая ссылка
Атигаев А.С. ИЗУЧЕНИЕ ЭЛЕКТРИЧЕСКИХ ХАРАКТЕРИСТИК ВОДНЫХ РАСТВОРОВ НЕКОТОРЫХ ЭЛЕКТРОЛИТОВ // Международный студенческий научный вестник. 2017. № 6. ;URL: https://eduherald.ru/ru/article/view?id=17854 (дата обращения: 07.04.2025).

