Целью исследования является определение наиболее эффективного и простого метода обнаружения превышений содержания вредных веществ в речной структуре с последующей разработкой устройства-анализатора.
В результате анализа различных методов исследования был определен наиболее простой и удобный в применении - электро-химический анализ проводимости воды.
Суть метода электро-химического анализа основывается на выявлении проводимости воды. Проводимость (величина, обратная сопротивлению) широко используется для определения содержания солей - важного показателя качества воды. Низкое содержание ионов в воде означает очень низкую проводимость, морская вода обладает высокой проводимостью.
Электрическая проводимость воды служит показателем уровня содержания в ней солей.
Сложно получить абсолютно чистую воду, так как вода - хороший растворитель. Даже дистиллированная вода самого высокого качества всегда имеет некоторое количество примесей, чаще всего - солей. Примеси, даже при низких концентрациях, позволяют воде проводить ток намного лучше, так как соли распадаются на свободные ионы, при помощи которых и передается ток.
Ход проведения эксперимента.
1. В неглубокую стеклянную посуду, объемом 1,2 литра, влить 0,5 литра воды (дистиллированной). Измерить электропроводность воды без примесей с помощью прибора, зафиксировать в журнале учета наблюдений.
2. Добавить в воду 50 миллиграмм хлорида свинца (II), тщательно перемешать. Произвести замер электропроводности, зафиксировать показания тока в журнал учета наблюдений. (прим. Работать со свинцом исключительно в защитной одежде, перчатках и маске, во избежание негативного влияния частиц свинца на организм.)
3. Повторить пункт 2, увеличивая массу навески, растворенной в воде до 150, 250, 500 миллиграмм.
4. Тару опорожнить. Промыть проточной водой.
5. Провести опыт заново (пункты 1-4) с использованием сульфата калия, затем с хлоридом калия.
6. Повторить пункты 1-5 для водопроводной воды, затем для речной. Увеличение массы навески пропорционально увеличению объема воды.
Все показания тока логарифмируются, массы навески выражаем в миллиграмме эквивалентном:
Результаты проведения опыта.
Логарифмированные показания тока и масса навески
р. Упа
PbCl2
|
2 см |
5 см |
10 см |
мг/экв |
|
-0,36 |
-0,56 |
-0,87 |
0 |
|
-0,34 |
-0,56 |
-0,87 |
0,36 |
|
-0,3 |
-0,53 |
-0,79 |
1,08 |
|
-0,19 |
-0,43 |
-0,53 |
1,8 |
|
-0,02 |
-0,22 |
-0,33 |
3,6 |
K2SO4
|
2 см |
5 см |
10 см |
мг/экв |
|
-0,36 |
-0,56 |
-0,87 |
0 |
|
-0,33 |
-0,55 |
-0,87 |
0,58 |
|
-0,21 |
-0,51 |
-0,71 |
1,72 |
|
-0,16 |
-0,43 |
-0,55 |
2,87 |
|
-0,14 |
-0,04 |
-0,21 |
5,75 |
KCl
|
2 см |
5 см |
10 см |
мг/экв |
|
-0,36 |
-0,56 |
-0,87 |
0 |
|
-0,25 |
-0,49 |
-0,63 |
1,35 |
|
-0,16 |
-0,22 |
-0,51 |
4,05 |
|
0,17 |
0,03 |
-0,21 |
6,76 |
|
0,53 |
0,32 |
0,11 |
13,51 |
Водопроводная вода
PbCl2
|
2 см |
5 см |
10 см |
мг/экв |
|
-1,56 |
-1,66 |
-1,72 |
0 |
|
-1,35 |
-1,43 |
-1,47 |
0,18 |
|
-0,97 |
-1,17 |
-1,43 |
0,54 |
|
-0,51 |
-0,87 |
-1,05 |
0,9 |
|
-0,25 |
-0,56 |
-0,92 |
1,8 |
K2SO4
|
2 см |
5 см |
10 см |
мг/экв |
|
-1,56 |
-1,66 |
-1,72 |
0 |
|
-1,14 |
-1,56 |
-1,61 |
0,29 |
|
-0,84 |
-1,14 |
-1,43 |
0,86 |
|
-0,55 |
-0,71 |
-1,05 |
1,44 |
|
-0,27 |
-0,37 |
-0,53 |
2,87 |
KCl
|
2 см |
5 см |
10 см |
мг/экв |
|
-1,56 |
-1,66 |
-1,72 |
0 |
|
-1,54 |
-1,66 |
-1,72 |
0,68 |
|
-1,47 |
-1,56 |
-1,61 |
2,03 |
|
-0,92 |
-1,31 |
-1,56 |
3,38 |
|
-0,46 |
-0,53 |
-0,89 |
6,76 |
Дистиллированная вода
PbCl2
|
2 см |
5 см |
10 см |
мг/экв |
|
-2,3 |
-2,53 |
-3,5 |
0 |
|
-2,3 |
-2,52 |
-3,22 |
0,36 |
|
-1,61 |
-1,72 |
-1,89 |
1,08 |
|
-1,51 |
-1,61 |
-1,72 |
1,8 |
|
-0,92 |
-1,2 |
-1,51 |
3,6 |
K2SO4
|
2 см |
5 см |
10 см |
мг/экв |
|
-2,3 |
-2,53 |
-3,5 |
0 |
|
-1,72 |
-1,89 |
-2,3 |
0,58 |
|
-0,94 |
-1,24 |
-1,5 |
1,72 |
|
-0,67 |
-0,94 |
-1,11 |
2,87 |
|
-0,05 |
-0,45 |
-0,55 |
5,75 |
KCl
|
2 см |
5 см |
10 см |
мг/экв |
|
-2,3 |
-2,53 |
-3,5 |
0 |
|
-1,72 |
-2 |
-2,82 |
1,35 |
|
-1,61 |
-1,89 |
-2,71 |
4,05 |
|
-1,39 |
-1,67 |
-2,49 |
6,76 |
|
-0,51 |
-0,79 |
-1,61 |
13,51 |
2 см
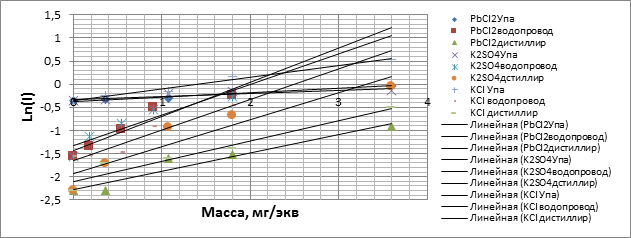
5 см
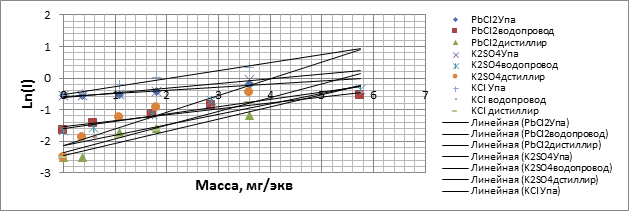
10 см
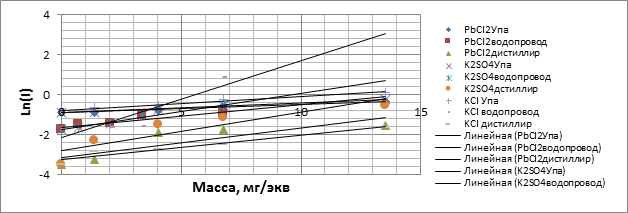
Из полученных результатов можно сделать следующие выводы.
Самое динамичное изменение показаний происходит при наиболее близком расположении электродов, а на расстоянии в 10 см результаты наиболее сглажены. Наиболее активным веществом, из используемых в опыте, является хлористый калий. Рост величины тока на расстоянии 10 см между электродами для дистиллированной воды составил 1,62, для водопроводной - 5,2, для воды из реки Упа - 1.
Использование данного метода позволит производить экспрес анализ речных систем с целью обнаружения точек загрязнения и в дальнейшем обеспечит возможность наиболее рационального природопользования.

