Введение
Транспортный сектор является вторым крупным потребителем энергоносителей в мире. За период 2005-2013 годы выбросы выхлопных газов с парниковым эффектом увеличились в мире на 49%. Прогнозируется, что в связи с ростом объема пассажирских и грузоперевозок, выбросы в будущем увеличатся. В подтверждение вышесказанного следует отметить, что общее количество автомобильных единиц сильно выросло в 2009 году, это количество достигло до 106 единиц. При этом годовой расход топлива составляет более 9×106 т, в том числе 2,5×106т дизельного топлива. Естественно, такого объема потребления невозможно удовлетворить только с переработки первичных источников. Следовательно, возникает необходимость на производство бензина из вторичных источников переработок, а именно бензина термического крекинга, каталитического крекинга и процесса коксования.
Увеличение содержания перекисей и смол в бензинах вызывает снижение их октановых чисел и повышение кислотности, которые коррозируют топливоподающую аппаратуру двигателя. Поэтому одним из важнейших эксплуатационных свойств автомобильных бензинов является их высокая химическая стабильность. Наиболее эффективным и экономически выгодным способом повышения химической стабильности топлив является применение антиокислительных, диспергирующих или комплексных присадок и деактиваторов металлов, добавляемых для подавления каталитического действия металлов на процесс окисления.
В настоящее время в нефтеперерабатывающей промышленности применяются различные антиокислительные присадки, качество которых во многом не удовлетворяет промышленный спрос из-за недостатков, связанных с плохой растворимостью в бензине, высокой вымываемостью водой и высокой их стоимостью, что делает их применение затруднительным. С другой стороны, в перспективных автомобильных бензинах содержание ароматических углеводородов неуклонно повышается, а содержание олефинов снижается. В связи с этим для стабилизации бензинов нужны более дешевые антиокислительные присадки, которые удовлетворяли бы все требования.
Целью работы является уменьшения загрязнения атмосферы за cчет изыскания новых эффективных и дешевых антиокислителей, испытание их в бензинах, содержащих непредельные углеводороды и антидетанационные присадки. В работе изучен механизм действия испытуемых антиокислителей, исследованы деактивирующие свойства некоторых гетероциклических соединений, а также изучено влияние исходных и стабилизированных бензинов с присадками на экологические параметры двигателя.
1. СОВРЕМЕННОЕ СОСТОЯНИЕ ВОПРОСА ПО СТАБИЛИЗАЦИИ ТОПЛИВА ВТОРИЧНОГО ПРОИСХОЖДЕНИЯ
1.1. Влияние углеводородного состава и различных факторов на химическую стабильность бензинов
Товарные автомобильные бензины очень разнообразны по своему углеводородному составу, что связано с различным содержанием в них продуктов, полученных путем вторичной переработки нефтепродуктов.
Углеводородный состав автомобильных бензинов зависит от технологии процесса, от качества исходного сырья и от режима переработки. В бензинах жидкофазного термического крекинга и коксования содержание непредельных углеводородов обычно составляет 30-45%, ароматических и нафтеновых 6-16%, а в каталитическом крекинге содержание непредельных углеводородов для различных ступеней колеблются в переделах от 13 до 14%. В отличие от бензинов термического крекинга, в каталитическом крекинге парафиновых углеводородов изостроения содержится значительный процент.
Результаты анализа группового состава непредельных углеводородов в прессдистилляте термического крекинга показывают, что с повышение температуры кипения фракций содержание олефиновых углеводородов в них снижается, а циклоолефиновых – возрастает, алкенил – ароматические углеводороды во фракциях, выкипающих до 122°С, отсутствуют, а в более высококипящих фракциях их содержание составляет 9-27% от общей суммы непредельных углеводородов.
1.2. Антиокислители металлов
Окисление углеводородов бензина начинается с образования свободных радикалов гидроперекисей, которые являются инициаторами цепной реакции:
инициаторами цепи: RH → R + H
раскрытие цепи: R′ + O2 → ROO′ ;
ROO′ + RH → ROOH + R
разветвление цепи: ROOH → RO′ + ′OH.
Назначение антиокислителя заключается в подавлении или полном устранении стадий распространения разветвления цепи, т.е. обрыва цепи вследствие взаимодействия антиокислителя со свободными радикалами. Обрыв цепи обусловлен передачей атома водорода или электрона промежуточному перекисному радикалу с образованием сравнительно стабильных продуктов. В качестве присадок, подавляющих образование перекисных цепей и радикальные реакции других реакционноспособных компонентов топлива, применяются некоторые арилалкиламины.
Эффективность антиокислителей сравнивалась по отношению к эффектинвности соединения 26В 4М. Сравнительные оценки стабилизирующей эффективности алкилфенолов показывают, что большое значение имеют природа и положение заменяющих групп. Из трех исследованных положений 2,4 и 6 наибольшая эффективность достигается, если положение 4 занято метильной группой. Максимальный эффект с двумя алкильными группами получается, если группа в положении 2 является третичной бутильной, а в положении4 – метильной. Наибольший эффект получается в том случае, когда из орто- положений занимает трет- бутильная группа. Высокая эффективность 2416В и 26В 4М, а также и некоторых других подобных им соединений в значительной степени объясняется тем, что в таких фенолах функциональная группа ОН защищена разветвленными трет- бутильными радикалами, которые затрудняют ее участие в побочных реакциях окисления.
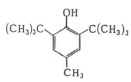
2,6 – ди-трет-бутил-4-метилфенол(26В 4М)
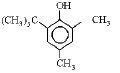
2,4-диметил-6-трет-бутилфенол(24М 6В)
Из бис фенольных соединений лучшими оказались 2,2-метил-бис-(4-метил-6-трет-бутилфенол) (2В 4М 6Г) и 4,4-метил-бис-(2,6-ди-трет-бутилфенол)(26В 4Г). Эти соединения оказались почти на 25% активнее, чем 26В 4М, но при хранении ведут себя хуже, чем стабилизированные 26В 4М. Указанные соединения имеют низкие летучести и не применяются для стабилизации топлив. Из производных нафталина высокие стабилизирующие свойства имеют нафтанол. При использовании α-нафтола возрастает содержание фактических смол, поэтому он в промышленности не применяется. Из других соединений нафталинов 1,5- и 1,7-диокси-нафталин имеет наиболее высокие стабилизирующие значения. Но он очень плохо растворяется в бензине.
В качестве ингибитора для стабилизации бензинов – крекинга испытывались различные NN-замещенные и п-фенилендиамины. Испытания проводились на смеси гидроочищенного бензина термического крекинга по методу, предусматривающему получение индукционного периода бензина порядка 300мин. В качестве эталона был использован NN-ди-втор-бутил-п-фенилендиамин, эффективность которого была принята за единицу.Наиболее эффективными являются те замещенные соединения (NN-1,2,3,12), в которых атом водорода каждой группы замещен на вторбутиловый, изопропиловый или фенольный радикал.
2. СИНТЕЗ И МЕТОДЫ ИССЛЕДОВАНИЯ ПРИСАДОК
2.1. Синтез и некоторые физико-химические свойства исследованных антиокислителей и деактиваторов металлов
На основе литературного материала в качестве присадок для стабилизации автомобильных бензинов исследованы и применяются алкилфенолы, аминофенолы, ароматические амины и шиффовые основания. Наиболее эффективными из них являются антиокислители, у которых аминогруппы и фенольный гидроксил находятся только в активных α- или пара-положениях.
В отечественной нефтеперерабатывающей промышленности для химической стабилизации автомобильных бензинов применяются три антиокислительные присадки: фракций фенолов из подсмольных вод полукоксования углей ФЧ-16, древесно-смольный антиокислитель – ДСА и параоксидифениламин – ПОДФА. Все указанные антиокислители имеют ряд существенных недостатков, один из них связан с плохой растворимостью в бензине, что делает нежелательным их применение в перспективных бензинах.
В последнее время на нефтеперерабатывающих заводах наблюдается выпадения смолистых осадков на дно бензиновых резервуаров. Эти осадки обнаруживаются в дренажных водах, в трубопроводах, по которым антиокислитель ФЧ-16 вводится в бензин, а также в трубопроводах, ёмкостях до их сжигания в двигателе. Указанными смолистыми веществами являются или компоненты антиокислителя ФЧ-16, нерастворимые в бензине , или же непосредственно сам антиокислитель.
Применяющийся в настоящее время в некоторых случаях древесно-смольный антиокислитель не обеспечивает достаточно высокую химическую стабильность автомобильных бензинов при длительном хранении.
Параоксидифениламин, добавляемый в качестве антиокислительной присадки к авиационным этилированным бензинам, плохо растворим, дорог, поэтому применение его нецелесообразно. Из этого следует, что вопрос выбора доступных для промышленного производства и эффективных антиокислителей назрел, актуален и имеет большое значение. В вышеизложенных соединениях дей1ствие антиокислителя в реакциях окисления связано, в первую очередь, с легкостью отрыва атомов активного водорода в аминных и гидроксильных группах антиокислителей.
2.2. Фурфурилалкиламины
Синтез фурфурилалкиламинов осуществляется путём конденсации фурфурола с алкиламинами под давлением водорода и в присутствии катализатора никель-ренея.
Например, получение α-фурфурилметиламина осуществляется следующим путем: в стальной вращающийся автоклав ёмкостью 600мл загружают 76,8г (66мл, 0,8моль) свежеперегнанного фурфурола, 24,8 (0,8моль)метиламина в 130мл метанола и 5-7 никеля-ренея.
После предварительной промывки водородом в автоклав подают водород под давлением 100-120атм. Процесс проводят при температуре 60-70°С до прекращения поглощения водорода. Гидрогенизат фильтруют от катализатора. Метанол отгоняют на водяной бане при слабом вакууме и остаток перегоняют при вакууме, собирая фракции с температурой кипения 40-42°С при 9 мм рт.ст., представляющим собой α-фурфурилметиламин. Выход равен 62-65г, что составляет 65-70% от теоретического. Из отогнанного растворителя получают дополнительно 8-10г фурфурилметиламина путем подкисления концентрированной соляной кислотой до рН 4-5 при охлаждении. После чего спирт отгоняют, остаток растворяют в небольшом количестве воды и подщелачивают твердой щелочью при охлаждении. Выделившееся масло экстрагируют нейтральным эфиром. Эфир отгоняют и остаток перегоняют в вакууме. Общий выход α-фурфурилметиламина составляет 75-80% от теоритического.
Температура кипения – 155-156°С
Плотность – 0,928 г/см3
Показатель преломления – 1,4440.
Некоторые физико-химические показатели синтезированных фурфурилалкиламинов приведены в таблице 1.
Таблица 1
Физико-химические показатели синтезированных фурфурилалкиламинов
|
Наименование веществ |
Температура кипения, °С |
n420 |
ρ420 |
|
α-фурфуриламин |
144-146 |
1,4586 |
0,941 |
|
α-фурфурилметиламин |
155-156 |
1,4440 |
0,0928 |
|
α-фурфурилэтиламин |
173 |
1,4523 |
0,936 |
|
α-фурфурилпропиламин |
197-198 |
1,4608 |
0,958 |
|
α-фурфурилбутиламин |
221 |
1,4673 |
0,967 |
|
Фурфурилфениламин |
54х |
- |
- |
|
х-температура плавления, °С |
|||
N-фурфурилалкилендиамины. Одно из основных требований к деактиватору металла заключается в том, чтобы он мог связывать в комплексные соединения ионы всех тех металлов, с которыми бензин соприкасается в условиях хранения, транспортировки и применения.
Наиболее эффективные присадки относятся к классу шиффовых оснований и представляют собой продукты конденсации салицилового альдегида с аминами. Эффективными деактиваторами металлов, представителями подобных соединений являются N,N′ – дисалицилиден-этилендиамин, N,N′ – дисалицилиденпропилендиамин и салицилиден –о- аминофенол. Основным недостатком этих деактиваторов является плохая растворимость их в топливах и индивидуальных углеводородах.
Фурфурол с диаминами и ароматическими аминами образуют соединения типа шиффовых оснований. На основе чего нами были синтезированы некоторые соединения шифовых оснований типа фурфурилалкилендиаминов, а также фурфурил-фенилендиаминов и исследованы в качестве деактиваторов металла в бензинах вторичного происхождения. Метод получения этих соединений осуществляется конденсацией реакционноспособного фурфурола с алкилендиамином.Реакция идет первичной конденсацией по карбонильной группе фурфурола с последующим гидрированием. Ниже приводится метод получения N-фурфурилэтилендиамина.
В качестве исходного сырья используются: этилендиамин (гидратная форма), фурфурол технический, водород элеткролитический и катализатор никель-рения. Условия получения: во вращающийся стальной автоклав ёмкостью 730 мл загружают раствор 87 г (1,11 моль) этилендиамина в 200 мл метанола, а затем при перемешивании туда же добавляют 34 г (0,354 моль) фурфурола, фурфурол должен быть свежеперегнанный и 8 г никель-ренея. Начальное давление водорода равно 100атм., температура гидрирования 80°С.
После прекращения поглощения водорода автоклав разгружают, катализат фильтруют, метиловый спирт и избыток этилендиамина тщательно отгоняет из колбы Вюрца на водяной бане при пониженном давлении. Метанольный раствор этилендиамина можно использовать для повторного синтеза. К остатку добавляют примерно 100 мл петролейного эфира, при этом выделяется коричневый осадок. Смесь сушат едким калием, затем эфирный раствор отфильтровывают от щелочи и осадка. Эфир отгоняют и осадок перегоняют в вакууме из колбы с колонкой Видемера, отбирая фракцией с температурой кипения 103-103,6°С при 10 мм рт.ст.
Выход N-фурфурилэтилендиамина равен 33,8 г, что составляет 68,2% от теоретического. Вещество представляет собой бесцветную умеренной вязкости жидкость со слабым аминным запахом. Фурфурилфенилендиаминовые соединения очищают путем перекристаллизации и высушивают в воздухе. Синтезированные нами диамины хорошо растворяются в эфире, спирте, индивидуальных углеводородах и бензине, а фенилендиамины плохо растворяются в бензине. В таблице 2 приводятся некоторые физико-химические свойства синтезированных фурфурилалкилендиаминов.
2.3. Методы исследования стабильности топлив по анализу продуктов окисления
Перекисное число. Показатель перекисного числа основан на определении активного кислорода, образовавшегося во время окислительных процессов в виде соединения, связанных двумя атомами кислорода. Один из атомов кислорода является активными и легко отрывается. Перекисное число выражается в мг активного кислорода, отнесенного к 100мл топлива.
Наиболее широкое распространение получили станнометрический, йодометрический методы определения перекисных чисел. Первый основан на определении количества хлористого олова, необходимого для расщепления перекиси:
R-OOH-H + SnCl +2HCl → R-O-H + SnCl4 + H2O
Непрореагированное хлористое олово оттитровывается 0,1Н водным раствором хлорного железа в присутствии индигокармина до неисчезающей при взбалтывании сине-зеленой окраски:
SnCl2 + 2FeCl3 → SnCl4 + 2FeCl2
Потенциометрическое определение перекисных чисел производилось следующим образом. 10 мл бензина, подлежащего анализу, растворяется в смеси, состоящей из 20 мл абсолютного изопропилового спирта и 2 мл ледяной уксусной кислоты. Затем к раствору добавляется 10 мл насыщенного раствора NaJ в абсолютном изопропиловом спирте и кипятят на бане 5мин, после чего к раствору добавляется 5 мл воды и медленно производится потенциометрическое титровании 0,1 раствором тиосульфата, с использованием лампового потенциометра «ЛП-5». В качестве электродов использовали платиновый каломелевый. Титрование производили в токе азота. До точки эквивалентности потенциал индикаторного электрода меняется очень мало.
Перекисное число выделившегося бензина вычисляют по формуле:
n.r.= 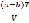 × 100 ; мг О2/ 100мл,
× 100 ; мг О2/ 100мл,
где a – объем 0,1 раствора тиосульфата натрия, израсходованного на титрование с испытуемым бензином, мл;
б – то же в контрольном опыте, мл;
Т – титр 0,1 раствора тиосульфата натрия, в граммах йода;
V – объем бензина, л.
Таблица 2
Физико-химические свойства синтезированных фурфурилалкилендиаминов
|
Исследуемое вещество |
Внешний вид и физическое состояние |
Температура, °С |
ρ420 |
nd20 |
|
|
кипения |
плавления |
||||
|
N-фурфурилэтилендиамин |
Бесцветная жидкость |
236 |
- |
1.0470 |
1.5029 |
|
N-фурфурилпропилендиамин |
Бесцветная жидкость |
271 |
- |
1.0760 |
1.5811 |
|
N-фурфурил-о-фенилендиамин |
Светло-жёлтые кристаллики |
- |
96 |
- |
- |
|
N-фурфурил-п-фенилендиамина |
тоже |
- |
106 |
- |
- |
Таблица 3
Физико-химические свойства стабилизируемых бензинов
|
Показатели |
Бензин термического крекинга. Обр.1 |
Бензин каталитического крекинга. Обр.2 |
Бензин термического риформинга. Обр.3 |
|
Фракционный состав,°С: 50% Плотность, г/см3 Йодное число, г J/100мл Содержание непредельных углеводородов, %вес. Индукционный период, мин Содержание фактических смол, мо/100мл Кислотность, мг/100мл Октановое число |
117 0,7309 96 43,7 130 3 0,0560 68 |
128 0,7628 38 21,8 210 4 0,150 76,6 |
109 0,7294 74 32,5 55 3 0,078 71,2 |
Кислотность. При жидкофазном окислении топлив одним из продуктов реакции является органическая кислота. Для определения кислотности широко применяются методы химического (ГОСТ-5985-80) и потенциметрического (ГОСТ-17834-82) титрования. Кислотность топлива выражается в мг едкого калия, израсходованного на нейтрализацию 100мл испытуемого нефтепродукта. Согласно ГОСТ 5985-80, кислотность определяют титрованием, применяя в качестве индикатора нитрозиновый желтый в виде 0,5%-го водного раствора. 50 мл испытуемого топлива кипятят в течение 5 мин с таким же объемом нейтрализованного 89% этиловго спирта, и в горячем состоянии титруют 0,05Н спиртовым раствором едкого калия до перехода желтой окраски в зеленую.
Заключение
На основании результатов исследований выявлено, что α-фурфурилпропиламины по механизму антиокислительного действия относятся к антиокислителям 2-й гуппы, которые воздействуют не только на стадию образования окислительных цепей, ко и тормозят вырожденное разветвление некоторых реакций. Добавление α-фурфурилпропиламина в бензин термического крекинга на разных стадиях старения способствует замедлению процесса смолообразования. После 50 дней хранения исходного крекинг-бензина его индукционный период снижается с 70 до 40 мин.
Результаты исследований показывают, что при сочетании ПОДФА и α-фурфурилпропиламина стабилизирующая эффективность по индукционному периоду повышается в 2,5раза.
Наиболее высокая стабилизирующая эффективность по повышению индукционного периода и торможению смолообразования появляется при сочетании α-фурфурилпропиламина с ионолом. Длительное хранение образцов топлив, стабилизированных парными антиокислителями 0,03% ФЧ-16 и 0,02% α-фурфурилпропиламином в жарких климатических условиях показывает, что срок хранения бензинов до образования 10 мг фактических смол удлиняется от 15 до 215 суток. За этот срок повышение кислотности и снижение октановых чисел бензинов не наблюдается. На основании полученных данных выявлены возможности применения парных антиокислителей α-фурфурилпропиламина с ФЧ-16 или ионолом для химической стабилизации бензинов на нефтеперерабатывающих заводах.
Результаты лабораторных укрупненных исследований парных антиокислителей деактиваторов металлов дают право судить о возможности практического применения исследованных композиций присадок для стабилизации автомобильных бензинов в нефтеперерабатывающей промышленности. В связи с чем, нами были проведены испытания влияния исследуемых добавок на коррозионную агрессивность бензина и на отложения во впускной системе двигателя. Все эти испытания дали положительные результаты и показали, что рекомендуемые композиции антиокислителей и деактиватор металлов не влияют на эти свойства.
Полученные данные показали, что N-фурфурил-этилендиамин является эффективным деактиватором еталлов, который полностью восстанавливает индукционный период до исходного уровня в присутствии металлов. На основании проведенных исследований следует рекомендовать композицию антиокислителей для стабилизации автомобильных бензинов в концентрациях: α-фурфурилпропиламина 0,01 – 0,05% вес. с ФЧ-16 и ионолом 0,014 – 0,05% вес. в зависимости от непредельных бензинов и деактиватора металлов – N-фурфурилэтилен диамина в концентрациях 0,01-0,02% вес.
Предварительный экономический расчет показал, что от внедрения парных антиокислителей, за счет уменьшения концентрации присадки даст экономию около 3,2 млн. тенге (около 15 тыс.$) на 1 млн. тонн крекинг-бензина.

