Специалисты в области микробиологии, цитологии и эмбриологии давно задавались рядом вопросов: каким образом происходит выбор клеткой своего жизненного пути? Почему возникают организмы, пораженные конгенитальными патологиями? Что способствует отклонению развития от нормы? Каким образом эти процессы могут быть связаны с канцерогенезом? Ответы на данные задачи учёные получили в ходе детального исследования микроокружения клеток, а также механизмов межклеточного взаимодействия, среди которых особую роль играют трансмембранные рецепторы семейства Notch.
Белки семейства Notch — интегральные белки-рецепторы, у человека представленные четырьмя типами (Notch 1-4). Данные белки осуществляют контроль пролиферации, дифференцировки и развития клеток и тканей, а также активируют транскрипцию генов, участвующих в регуляции баланса между этими процессами [1].
В 1913 г. в ходе исследования дифференцировки эктодермы, проводимых на экспериментальной форме Drosophila melanogaster, американским биологом Томасом Хантом Морганом были открыты белки-факторы роста, играющую особую роль в созревании и функционировании клетки. Позднее были получены сведения о нарушениях развития D. melanogaster в случае повреждения участков гена NOTCH (Дж. С. Декстер, 1914 г.) и участии сигнального пути Notch в онтогенезе (Д. Полсон, 30-е гг. XX века) [2].
Строение рецепторов сигнального пути Notch удалось изучить лишь после клонирования и секвенирования гена. Было установлено, что данные белки представляют собой огромные молекулы-димеры, имеющие молекулярную массу в пределах 300 кДа, содержащие специфические для данного семейства внутриклеточный и внеклеточный домены с множественными (от 26 до 29) EGF-подобными повторами, способными связывать лиганд [1, 2].
Активация сигнального пути Notch является уникальной. Она происходит при непосредственном физическом контакте данных белков с клетками, содержащими на своей поверхности лиганды к Notch-белкам. У млекопитающих описано 7 родственных друг другу лигандов (семейства Delta, Serrate и Lag-2 (DSL), Serrate-like ligands (Jagged1, Jagged2), Delta-like ligands (DLL1,-3,-4), каждый из которых является трансмембранной формой белков, обеспечивающих взаимодействие соседних клеток друг с другом. Связь между Notch-белками и данными лигандами была доказана в работе, проведенной на Caenorhabditis elegans, выявившей взаимосвязь интегрального белка γ-секретазы и сигнального каскада Notch. Это открытие позволило ученым предположить, что после контакта рецептора Notch со специфичным ему лигандом происходит отщепление внутриклеточного домена данного рецептора N-IC (Notch Intracellular Domain, NICD), транспорта домена в ядро, где начинается активация транскрипции генов семейств HES и HEY, ответственных за специализацию и жизненный цикл клетки [1].
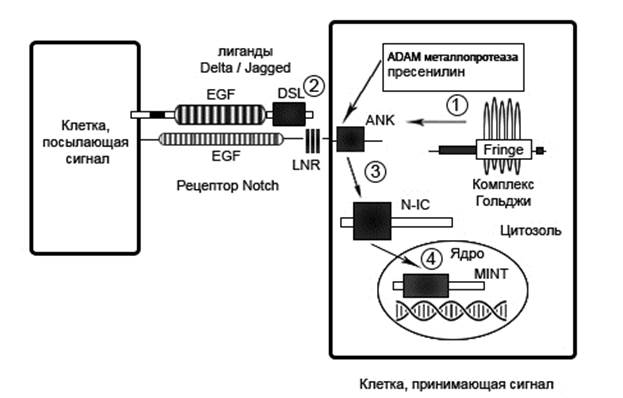
Рис. 1. Каноническая активация сигнального пути Notch. На схеме указаны основные участники и некоторые целевые гены. 1 — Рецептор Notch расщепляется фуриноподобной протеазой в комплексе Гольджи и переносится на клеточную поверхность в качестве гетеродимера. Возможно его гликозилирование белками Fringe аппарата Гольджи. 2 — После экспрессии на поверхности клетки Notch взаимодействует с лигандами (DSL, Jagged1 и др.). 3 — После связывания лиганда с рецептором лиганд расщепляется металлопротеазой ADAM и γ-секретазой для освобождения N-IC. 4 —N-IC инициирует свои последующие эффекты путем миграции на ядро и связывания с его элементами.
Активация данного пути является сверхточным процессом. Это доказали исследования, проводимые на экспериментальных животных. Согласно полученным данным, выбор правильного клеточного пути во многом зависит от баланса между количеством рецепторов и лигандов к ним. К примеру, недостаточность Jagged1 вызывает пороки развития многих систем органов у людей [1].
Учёные выделяют две категории белков-регуляторов сигнального пути: активаторы и ингибиторы. К первым можно отнести ядерные белки Deltex и MINT: в зависимости от контекста они определяют, стоит ли экспрессировать тот или иной ген. Среди супрессоров транскрипционных механизмов наиболее изучены LNX, SEL-10, Numb и Itch [2].
Присоединение остатков сахаров к молекулам Notch-белков, а также их лигандам при помощи Fringe действует в роли критического регулятора активации сигнального пути. Посредством модификации EGF-подобных повторов происходит усиление Delta сигналов и подавление Serrate. Таким образом на клеточном уровне организации удаётся разграничить друг от друга несколько видов тканей и сохранить их специфичность. На данный момент установлено лишь три белка, относящихся к Fringe-комплексу. Это LFng, MFng и RFng. Посредством экспериментов на мышах было выявлено, что LFng особенно необходим для дифференцировки сомитов в области будущей грудной клетки и позвоночника [2, 7].
Процесс активации сигнального пути Notch в разных тканях неодинаков. Различия объясняются типом ткани, клеточного окружения, сигнала, лиганда и степенью содержания белков семейства Notch в данной клетке [8].
На данном этапе исследований остаётся неизвестным, усиливают ли гены-компоненты сигнального пути Notch потенциал к тканеспецифичной дифференцировке или ингибируют его. Опубликованы противоречивые данные, связанные со спектром действия белков Notch на дифференцировку клеток. Например, при контакте NICD человеческих мультипотентных мезенхимных стволовых клеток (ММСК) с лигандом семейства Jagged1, транскрибированного при участии экзогенного белка Jag1, ведёт к усилению межклеточного взаимодействия, т.е. активации остеогенного клеточного дифферона ММСК. Введение же активированного домена NICD в ММСК мыши in vitro приводит к подавлению дифференцировки остеогенных клеток, а in vivo — к снижению плотности массы костной ткани [2].
Важны Notch и для уже дифференцированных клеток. Доказано, что связывание DSL лигандов с активированными Notch-рецепторами обеспечивает такие процессы, как клеточная память и синаптическая пластичность нейронов. Кроме того, передача сигналов Notch регулирует дифференцировку клеток-составляющих нейроглии и арборизацию (т.е. ветвление наподобие дерева) нейронов [3].
Влияние типа активированного рецептора на Notch-эффект демонстрируется следующим образом: стимуляция Notch1 ингибирует процесс созревания зрелых остеолкастов, в то время как активирование Notch2 приводит к усиленному остеокластогенезу [7].
Также при дифференцировке клеток имеет значение момент действия Notch-белка. Так, решающим регулятором судьбы развивающегося кардиомиоцита может стать своевременная активация доменов Notch1, -4, вырабатываемых эндотелиоцитами васкуляризирующих тканей. Через множественные взаимодействия будущего миокарда с нервным гребнем данные гены приводят к развитию внутренней сердечной оболочки и морфогенезу сердечных клапанов и камер. Notch также необходимы для дифференцировки коронарного сосуда. Однако, взаимодействие рецепторов Notch с лигандом HEY2 на более позднем этапе может повлечь недоразвитие сердечных клапанов и возникновение аритмии [5]. Учёные предполагают, что для запуска подобных каскадных реакций необходим своеобразный пороговый уровень сигнализации Notch пути. Превышение или недостаточная степень реагирования на лиганды приводят к инактивации сигналов определения жизненного пути клетки. Таким образом осуществляется регуляция стволовых свойств мультипотентных клеток или их дифференцировка на генетическом уровне [1].
Известно, что мутации доменов, входящих в сигнальный путь Notch, приводят к серьёзным заболеваниям опорно-двигательного аппарата (остеопения, остеосаркома, дизостоз, брахидактилия). Зачастую это происходит вследствие формирования искажённого набора соматических границ в эмбриогенезе. Причиной такого явления становится нарушение периодичности активации генов, участвующих в передаче Notch-сигналов (HES1, DLL1, -3) [7,8].
Выделяют ряд целевых генов Notch-белков, которые определяют направление сигнального пути Notch. Регуляторами клеточного цикла являются CyclinD1, NRARP, NF-κB, TP21, pre-Tα. Маркерами злокачественных новообразований служат C-MYC, IGF1-R, SURVIVIN, SLUG. Белки HES1 и HEY1 являются не только непосредственными мишенями для сигнального пути Notch, но также действуют как ингибитор транскрипционных процессов, тем самым регулируя клеточный цикл [2].
Семейство Notch осуществляет контроль над эмбриональным развитием не только в виде определения направления развития клетки, но также посредством пары механизмов. Первый получил название латеральная спецификация. Она происходит, когда клетки одного типа одновременно задействованы как в экспрессии белков и лигандов, так и в принятии их сигналов на одной стадии активации Notch пути. Обычно данный процесс характеризуется выраженной асимметрией, поскольку клетка самостоятельно выбирает, какое соединение и в каком объеме ей необходимо секретировать. При этом клетка, проходящая этапы дифференцировки (например, в нейробласт), ингибирует аналогичные процессы у соседних клеток. В будущем это отразится следующим образом: 1) произойдёт разделение специфических клеточных типов друг от друга; 2) будут сформированы границы между тканями. Второй способ — индуктивная передача сигналов — заключается в экспрессии белков и их лигандов клетками двух различных типов, т.о. удаётся осуществить активацию Notch только в тех клетках, плазмалемма которых несёт на своей поверхности Notch-рецепторы. [1, 2, 5].
Определённую роль белки Notch играют также и в коррекции процессов гемопоэза, который являет собой баланс между самообновлением и дифференцировкой кроветворных стволовых клеток. Гемопоэтические ткани и органы обычно богаты данным типом белков. Здесь сигнальный путь Notch активируется в ходе взаимодействия его рецепторов с лигандами Jagged1, DLL 1 и 4, которые несут на себе клетки стромы красного костного мозга. Экспрессируются они и в тимусе, что говорит о важности данного сигнального каскада для формирующихся Т-клеток. Активация генов Notch1 и Notch2 была обнаружена в гранулоцитах [6].
В ходе экспериментов учёными было показано, что гиперактивация семейства Notch-белков способствует возникновению различных форм неоплазий, вызванных нарушениями в структуре генов, ответственных за апоптоз клетки [5].
Перспективным направлением является изучение сигнального пути Notch как маркера клеточных патологий, в частности, канцерогенеза, поскольку Notch-белки контролируют ключевые процессы жизнедеятельности клетки. Характерной особенностью Notch является влияние на пролиферацию опухолевых клеток или её подавление в зависимости от микроокружения в пределах одной и той же опухоли [4].
В 1991 г. L.W. Ellisen вместе с соавторами доказали вовлеченность сигнального пути Notch в стимуляцию опухолевых процессов во время изучения на экспериментальном животном Т-клеточного острого лимфобластного лейкоза (Т-ОЛЛ). В ряде случаев нарушение структуры доменов Notch приводило к образованию химерного белка Notch 1/ TCRβ, имитирующего NICD. Позднее была обнаружена мутация гена Notch1, в 56% случаев приводящая к Т-ОЛЛ. В 31% мутации Notch1 обнаруживалась хроническая лимфоцитарная лейкемия (ХЛЛ). Предполагается, что для решения подобной проблемы может быть использована лиганд-независимая активация Notch-рецепторов. Она приведёт к стабилизации N-IC внутри гена, однако неблагоприятный прогноз по-прежнему будет сохраняться [4].
В крупных опухолях сигнальный путь Notch был впервые обнаружен в вирусе мышиной опухоли молочной железы, причиной которого считается мутация гена Notch4, а также повышенный синтез Notch1 и взаимодействие его с лигандом Jagged1 [6].
В целом, считается, что сигнальный путь Notch оказывает в основном проонкогенное действие, вызывая такие патологии, как Т-ОЛЛ, ХЛЛ, аденокарцинома легкого, рак молочной и поджелудочной железы, меланома [2]. В качестве опухолевого супрессора белки Notch действуют при связывании с лигандами на поверхности клеток, вызывающими плоскоклеточный рак кожи и рак шейки матки [4]. Потеря пресенилина — каталитической субъединицы γ-секретазы — способствует потере активности данного белка и развитию болезни Альцгеймера. Notch-белки также способствуют выживанию опухолевых клеток и их устойчивостью к химиотерапии [2].
Подводя итоги, можно сказать, что белки семейства Notch и инициируемый ими сигнальный путь являются уникальными среди всех белков человеческого организма. В зависимости от клеточного контекста белки Notch регулируют разнообразные интрацеллюлярные процессы, а в ряде случаев становятся причиной серьёзных мутаций. Дальнейшие исследования сигнального пути Notch могут быть использованы для разработки методики противоопухолевой терапии, создания и поддержания специфичных свойств стволовых клеток, искусственной регуляции таких процессов, как ангиогенез, гемопоэз и др., что делает это направление весьма перспективным.
Библиографическая ссылка
Кутузова Л.А., Меметова А.А., Силиверст О.Н. РОЛЬ БЕЛКОВ СЕМЕЙСТВА NOTCH В ЖИЗНЕДЕЯТЕЛЬНОСТИ КЛЕТКИ // Международный студенческий научный вестник. – 2018. – № 6. ;URL: https://eduherald.ru/ru/article/view?id=19271 (дата обращения: 27.04.2024).

